全球约有 3 亿罕见病患者,其中数千万属于极罕见病患者。传统药物研发模式难以满足他们的需求。
基因组编辑的出现为从根本上治疗罕见病提供了可能。包括 RNA 引导的核酸酶、重组酶及其工程化衍生物(如碱基编辑器、先导编辑器和表观遗传编辑器)在内的多种基因组编辑系统,如今能够在活细胞内对 DNA 进行精确修饰,为多种疾病提供了治疗潜力。
成为全球首位接受定制化碱基编辑疗法治疗的患者后,婴儿 KJ・Muldoon 如今已恢复健康,摆脱了罕见遗传代谢病带来的有毒氨蓄积 —— 该病在婴儿期的死亡率曾高达 50%。
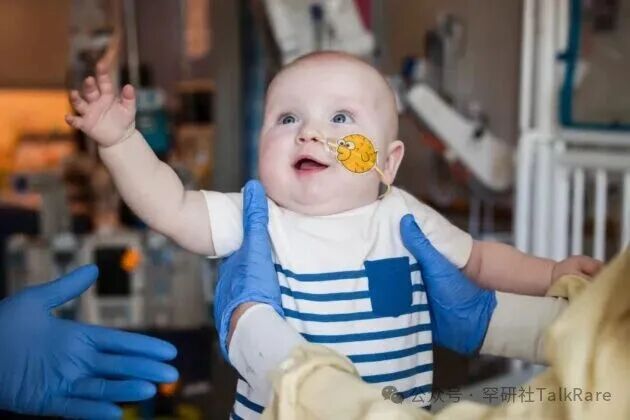
他的故事既彰显了基因编辑改变生命的巨大潜力,也凸显了该领域面临的重大挑战:
如何将这类疗法推广,让更多患者受益?
KJ 所患的尿素循环障碍,由两个单一致病突变引起,可被精准靶向。然而,许多遗传病是由散落在整个基因上的众多突变导致的,个体化修复的资源消耗极大,难以规模化。
麻省总医院(MGH)副研究员本・克莱因斯蒂弗(Ben Kleinstiver)博士在接受采访时表示:
在基因组可编程位点插入大片段 DNA 序列,有望成为一种通用型药物,无论患者携带何种致病突变,都能接受治疗。
他的团队近期取得重要进展,让大片段基因插入在治疗应用中变得更加安全。
在发表于《自然》的新研究《免疫逃逸型 DNA 供体与重组酶实现千碱基级基因写入》中,克莱因斯蒂弗团队与 Full Circles Therapeutics 合作,开发出一种环状单链 DNA(ssDNA)供体,可实现 kb 级整合,且对细胞无毒。

这项名为 INSTALL 的技术,为传统双链 DNA(dsDNA)供体提供了替代方案。
双链 DNA 虽能被重组酶等多种基因组编辑酶识别,但会强烈引发有害免疫反应。而 INSTALL 技术通过连接一小段双链 DNA 区域,既能保持与重组酶的兼容性,其长度又能避开胞质 DNA 感受器与免疫激活蛋白 cGas 的检测。
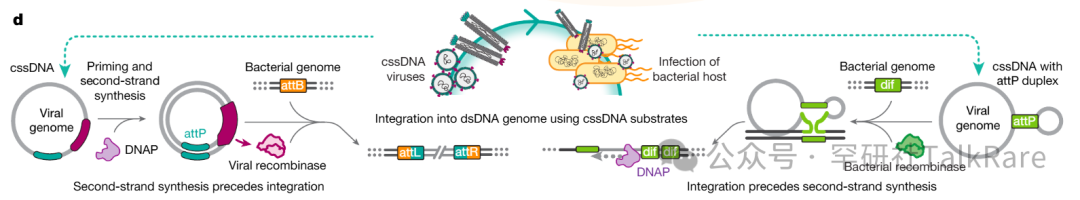
图:携带 cssDNA 基因组的病毒整合生命周期:在宿主 DNA 聚合酶(DNAP)对其基因组完成第二条链合成之前或之后,病毒利用自身编码或宿主编码的重组酶实现基因组整合。
实验结果显示:通过脂质纳米颗粒(LNP)递送,INSTALL 技术可在小鼠肝脏中成功、安全地实现大片段遗传物质的非病毒插入;与之对比,接受传统双链 DNA 分子的小鼠则出现了致死性免疫反应。
谈及该技术的起源,该研究第一作者、克莱因斯蒂弗实验室博士后研究员康纳・图(Connor Tou)博士回忆道:
尽管新型重组酶与转座酶技术不断涌现,但在规模化基因插入研究中,DNA 供体引发的先天免疫障碍似乎并未得到足够重视。
“我们知道单链 DNA 可以避开胞质内关键免疫感受器,但它与重组酶完全不兼容。” 图博士告诉记者。
“我们的‘顿悟时刻’是:大自然早已给出潜在方案—— 许多噬菌体和细菌天然使用环状单链 DNA 完成插入。我们只需要在哺乳动物细胞中重现这些机制。”
走向非病毒递送
重组酶对双链 DNA 供体的依赖,长期以来让病毒递送系统(如腺相关病毒 AAV)更具优势,这类载体可直接进入细胞核,避开胞质免疫识别。
但 AAV 载体存在明显局限:生产成本高、装载容量有限、会引发载体免疫,无法重复给药。这些局限推动了学界对大片段基因插入的非病毒递送方式的研究热情。
INSTALL 技术首次在人原代细胞与小鼠体内,通过 LNP 实现了非病毒、无毒的大片段序列插入。
不过,小鼠肝脏中成功整合 DNA 的细胞不足 1%。虽然对部分疾病而言,低水平修复已足够有益,但大多数疾病需要个位数至两位数级别的编辑效率才能让患者获益。
Basecamp Research 首席科学官约翰・芬恩(John Finn)博士认为,该研究在解决基因药物中双链 DNA 毒性这一关键问题上是 “重大突破”,但他预计 AAV 在短期内仍不会被取代。
距离临床转化仍需更多研究
不可否认,诸如向非分裂细胞的细胞核高效递送等下游难题,仍是临床转化的瓶颈。
“我们体内几乎所有重要细胞,包括脑细胞、肝细胞、肌细胞,大多都是非分裂细胞。” 芬恩告诉记者。“在这个问题解决之前,我认为该技术很难在临床上产生重大影响。”
Basecamp Research 一直积极利用 AI 赋能基因编辑技术。今年早些时候,该公司发布了 EDEN 系列 AI 模型,通过 9.7 万亿条进化数据训练,可设计用于大片段基因插入的可编程重组酶。
克莱因斯蒂弗也认同,提升整合效率是该研究未来的核心方向。
本研究使用的是递送 mRNA 的标准 LNP,载体可进一步优化,以适配新型环状单链 DNA 供体。
他还指出,重组酶核酸组分的工程化改造仍是一个有待深入挖掘的方向。
例如,在与环状单链 DNA 结合的短寡核苷酸上添加有助于核递送的化学修饰等手段,有望进一步提高整合效率。
图博士坦言,该研究目前仅为初步概念验证,距离临床应用仍需大量后续工作。
“我们乐观地认为,新一代 INSTALL 系统,结合持续的重组酶蛋白工程改造,将在不依赖突变类型的基因组编辑及其他应用中具备转化价值。”