杜氏肌营养不良症 (Duchenne muscular dystrophy, DMD) 是一种由抗肌萎缩蛋白 (dystrophin) 编码基因突变引起的X染色体连锁的隐性遗传病,临床表现为进行性肌肉萎缩,患者多于20岁左右死于心力衰竭或呼吸衰竭。目前,与DMD基因相关的变异已超过7000个,绝大多数为外显子区域的缺失、重复和点突变。据统计,DMD男婴发病率约1/5000-1/3500,已纳入我国《第一批罕见病目录》。尽管目前多款DMD疗法已经取得了突破性进展,但其发病机制复杂且治疗方法存在疗效有限、成本较高等问题,亟需进一步的研究和创新。
近日,Solid Biosciences公司宣布,其针对杜氏肌营养不良症 (DMD) 的潜在同类最佳 (best-in-class) 在研AAV基因疗法SGT-003已获得欧盟委员会 (EC) 授予的孤儿药资格认定 (ODD)。随着III期临床的开展和积极的监管进展,SGT-003的全球化研发战略进入加速落地阶段,也为全球DMD患者带来新的治疗希望。
差异化设计构筑同类最佳潜力,全球监管认可全面加持当地时间2026年4月28日,Solid Biosciences公司 (Nasdaq: SLDB) 宣布,其针对杜氏肌营养不良症 (DMD) 的潜在同类最佳 (best-in-class) 在研AAV基因疗法SGT-003已获得欧盟委员会 (EC) 授予的孤儿药资格认定 (ODD)。随着III期临床的开展和积极的监管进展,SGT-003的全球化研发战略进入加速落地阶段,也为全球DMD患者带来新的治疗希望。

▲ 新闻稿截图
DMD是一种致命的X连锁遗传病,由于抗肌萎缩蛋白 (dystrophin) 的缺失导致进行性肌肉退化。过去的几十年,DMD的治疗经历了从支持性治疗 (如物理治疗、呼吸支持) 到药物干预的演变。皮质类固醇 (如泼尼松、地夫可特) 是长期以来的标准疗法,它们能减缓肌肉力量的衰退,但副作用显著,无法从根本上改变疾病进程。以Sarepta Therapeutics公司的Exondys 51® (eteplirsen) 为代表的反义寡核苷酸 (ASO) 药物,通过“外显子跳跃”技术,跳过有缺陷的外显子,使得细胞能够翻译产生一个缩短但仍有部分功能的抗肌萎缩蛋白。2023年获批的Sarepta/罗氏的基因疗法Elevidys,则通过AAV载体将一个微型抗肌萎缩蛋白 (micro-dystrophin) 基因递送到肌肉细胞中,试图从源头上“修复”问题。
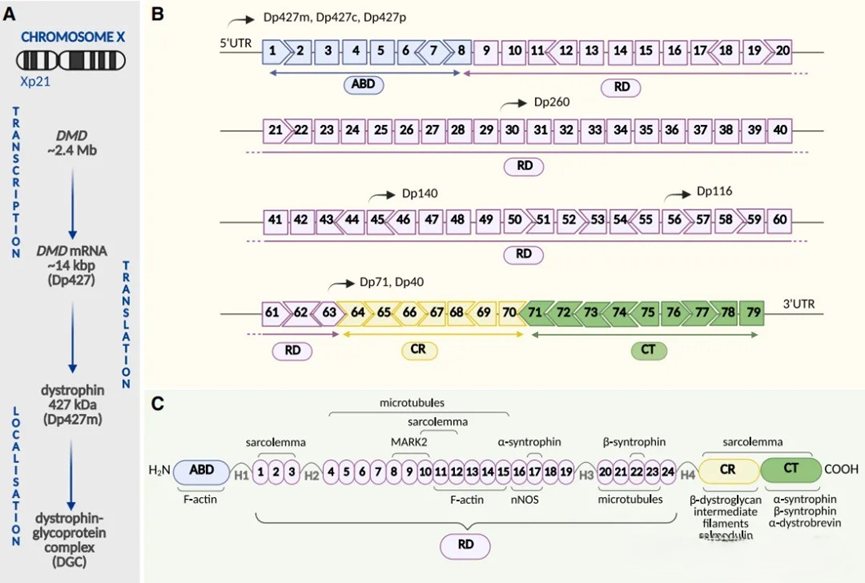
▲ DMD基因及其蛋白 (Łoboda A, 2025)
抗肌萎缩蛋白 (microdystrophin) 是抗肌萎缩蛋白相关蛋白复合物 (DAPC) 的关键组分,而DAPC是维持肌肉完整性的必需结构。SGT-003采用Solid公司专有的新一代肌肉靶向性AAV-SLB101衣壳,通过一次性静脉输注 (Intravenous, IV) 递送包含工程化的R16和R17 nNOS结合域的微型抗肌萎缩蛋白基因拷贝,旨在高效、靶向性地将治疗基因序列递送至肌肉组织,以期提高疗效并降低载体剂量及相关毒性风险。前期的非临床研究表明,nNOS可以改善肌肉血流,从而减少缺血和肌肉疲劳引起的肌肉分解。
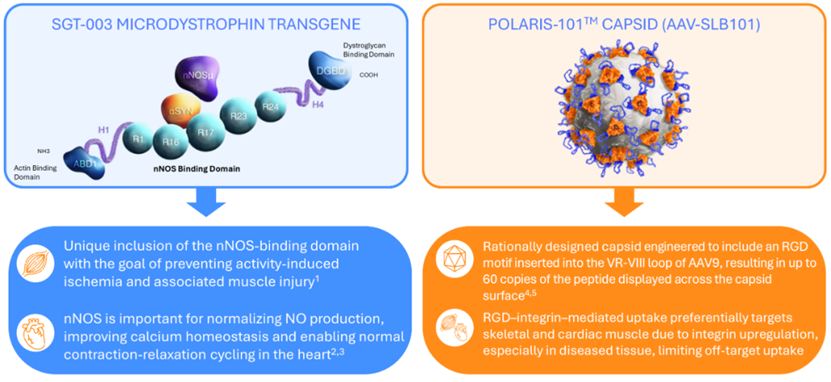
▲ SGT-003设计特点
传统AAV介导的DMD基因疗法普遍存在肌组织转导效率低、肝脏脱靶严重的问题,而SGT-003采用的AAV-SLB101衣壳蛋白实现了 “靶向增强 + 脱靶减少” 的双重突破;同时,传统微型抗肌萎缩蛋白疗法仅能实现蛋白功能的补充,而SGT-003通过nNOS结合域的设计,从病理生理角度改善肌肉的生存环境,实现了治疗效果的升级。这种基于疾病病理的差异化创新,成为破解行业痛点的核心关键,也为后续其他遗传病的基因疗法研发提供了重要参考。
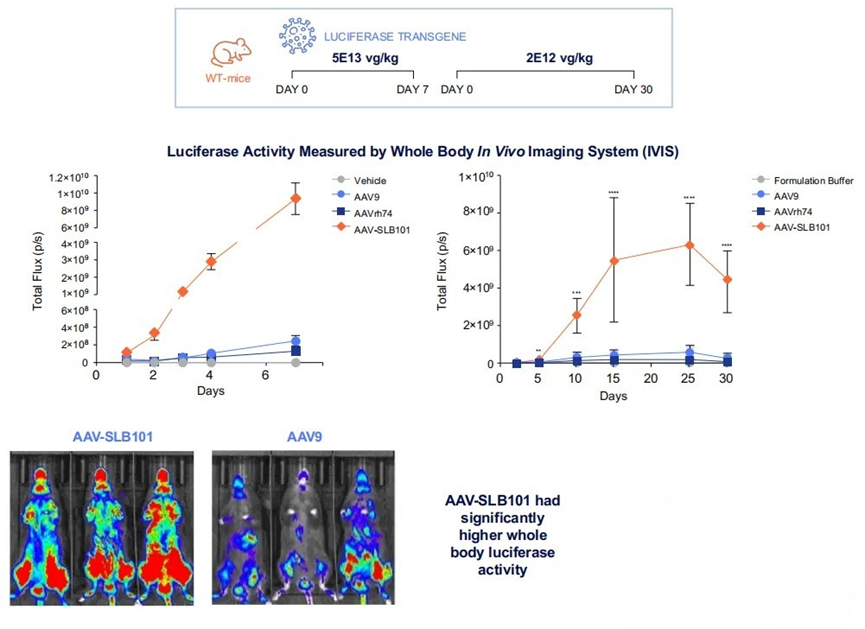
▲ AAV-SLB101与AAV9及AAVrh74动力学与转导效率对比
值得注意的是,已经接受过已批准的或在研基因疗法药物或基因编辑疗法的患者以及DMD基因外显子1至11缺失、外显子42至45或外显子57至69缺失的患者同样不适用于SGT-003。基于突破性的设计与早期临床数据,SGT-003此前已获得美国FDA授予的快速通道资格认定 (FTD)、孤儿药资格认定 (ODD) 、儿科罕见疾病资格认定 (RPDD),以及英国MHRA的创新许可和准入途径资格认定 (ILAP)。
全球化临床推进:双试验并行,覆盖全年龄段患者DMD是全球基因疗法研发的核心赛道之一,目前全球范围内已有多款在研药物处于不同临床阶段。为支撑全球多国同步获批,Solid正推进两项全球性、多中心临床试验,形成 “早期探索 + 确证性疗效” 的完整证据链:
INSPIRE DUCHENN (NCT06138639) 一项首次在人体进行的开放标签、单剂量、多中心Ⅰ/Ⅱ期临床试验,旨在评估SGT-003在DMD患儿儿中的安全性、耐受性和有效性。截至目前,已有36名受试者接受了SGT-003的单剂量给药,数据显示药物总体耐受性良好,未出现与药物相关的严重不良事件,这一结果与此前公布的中期数据一致,进一步验证了该药物的临床安全性。

▲ SGT-003Ⅰ/Ⅱ期临床试验结果
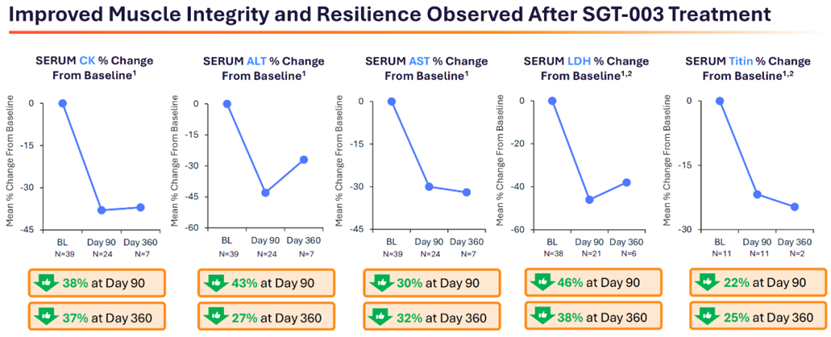
▲ SGT-003Ⅰ/Ⅱ期临床试验结果
IMPACT DUCHENNE (NCT07160634) 是一项随机、双盲、安慰剂对照Ⅲ期临床试验 ,核心入组人群锁定为7至12 岁可行走的DMD患儿,旨在为SGT-003的监管审批提供依据。试验的主要终点设定为18个月时受试者从仰卧位起身速度 (TTR) 较基线的变化,同时纳入了多项关键次要终点,全面评价药物对患者运动功能的改善作用。所有受试者将在SGT-003给药日期后接受至少5年的长期随访。