今日NMPA送达的药品送达信息显示,第一三共的盐酸吡昔替尼胶囊(Pexidartinib,PLX3397),遗憾收到通知件。
![]()
(图片来源:NMPA官网)
盐酸吡昔替尼最初由Plexxikon发现,后纳入第一三共体系开发。它是一个口服小分子酪氨酸激酶抑制剂,核心靶点是CSF1R(colony-stimulating factor 1 receptor),同时也抑制KIT和FLT3-ITD。其研发逻辑主要是针对TGCT(腱鞘巨细胞瘤) 中CSF1/CSF1R通路异常激活所驱动的滑膜巨噬细胞聚集和病灶增殖。
作为一款在罕见病腱鞘巨细胞瘤(TGCT)领域具有里程碑意义的“First-in-class”靶向药物,也是目前全球首个针对腱鞘巨细胞瘤(TGCT) 的靶向药物,该药基于ENLIVEN研究约38%的客观缓解率在2019年获FDA批准上市,商品名为Turalio,用于治疗伴严重病变或功能受限、且无法通过手术改善的症状性TGCT成人患者。
安全性方面,盐酸吡昔替尼最大的临床限制是肝毒性。FDA说明书和公司更新都强调,该药可导致严重甚至致命性肝损伤,因此美国实施了风险评估与管控策略(REMS)管理计划。
2020年,EMA对Turalio的上市申请作出了拒绝上市许可的意见。EMA给出的核心理由是:虽然研究中肿瘤缩小,但对疼痛和关节功能等症状改善幅度有限、持续性不够明确,同时存在不可预测且可能危及生命的肝毒性担忧,因此认为获益不大于风险。

(图片来源:EMA官网)
2022年FDA又批准了新的给药方案,并将部分长期随访数据纳入标签。当前美国标签所示推荐剂量为250mg、每日2次、随低脂餐服用;这一方案替代了早期的空腹高剂量给药,目的是降低因进食导致暴露升高和肝毒性风险。
东亚桥接研究方面,该药在2025年发表的NCT04488822结果显示:在40例东亚TGCT患者中,第25周RECIST评估的ORR为22.5%,TVS评估的ORR为 47.5%,关节活动度改善明显;作者认为其安全性与既往研究总体一致。
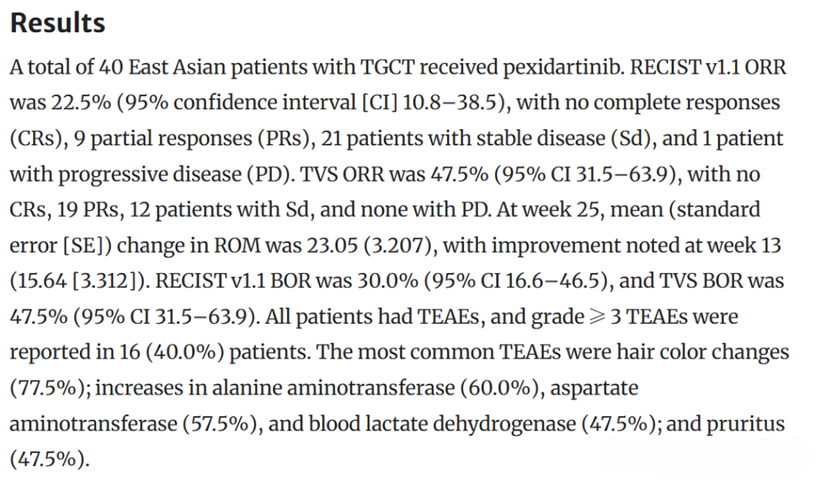
(图片来源:文献)
2025年1月,该药在中国提交了上市申请并获得优先审评,但如今遗憾未能获批,不知道是否是CDE参考了EMA的意见,同样评估认为该药的风险大于获益呢?