遗传性共济失调 (hereditaryataxia, HA) 是一大类具有高度临床和遗传异质性、病死率和病残率较高的遗传性神经系统退行性疾病。其中常染色体隐性遗传小脑性共济失调中最常见的弗里德赖希共济失调 (Friedreich ataxia, FA) 患病率为3~4/10万,在我国极为罕见,其发病机制是Frataxin (FXN) 基因的第1个内含子上GAA重复扩增导致其表达量减少所致。目前,仅有一款口服Nrf2激活剂Skyclarys获批上市,尚无针对FA心肌病的有效药物,亟需开发能够从根源上纠正基因缺陷的创新疗法。
近日,在刚刚结束的第75届美国心脏病学会科学年会 (ACC.26) 上,Lexeo Therapeutics公司发布了其针对弗里德赖希共济失调 (FA) 相关心肌病的在研AAV基因疗法LX2006( AAVrh.10hFXN) 极具潜力的I/II期中期临床数据。这是全球首个在临床中证实能有效干预FA相关心肌病的基因疗法,为广大患者带来了新的治疗希望。
临床数据双重获益:心脏指标逆转与神经功能稳定
近日,在刚刚结束的第75届美国心脏病学会科学年会 (ACC.26) 上,Lexeo Therapeutics (NASDAQ: LXEO) 公司发布了其针对弗里德赖希共济失调(Friedreich's ataxia, FA)相关心肌病的在研AAV基因疗法LX2006 ( AAVrh.10hFXN) 极具潜力的开放标签、剂量递增I/II期中期临床 (NCT05302271) 数据。结果表明,单次静脉注射LX2006即可恢复FA心肌病患者的心脏Frataxin蛋白水平,并有效改善心肌应激和重塑的关键标志物。这是全球首个在临床中证实能有效干预FA心肌病的基因疗法,为广大患者带来了新的治疗希望。

▲ 新闻稿截图
弗里德赖希共济失调 (Friedreich ataxia, FRDA) 是一种常染色体隐性遗传的进行性神经退行性疾病,主要由位于9q21.11上的Frataxin (FXN) 基因的第1个内含子上GAA重复扩增引起 (正常<33次,致病>66次),以儿童或青少年起病的肢体共济失调、腱反射消失、心肌病和糖尿病为特征,是最常见的遗传性共济失调。
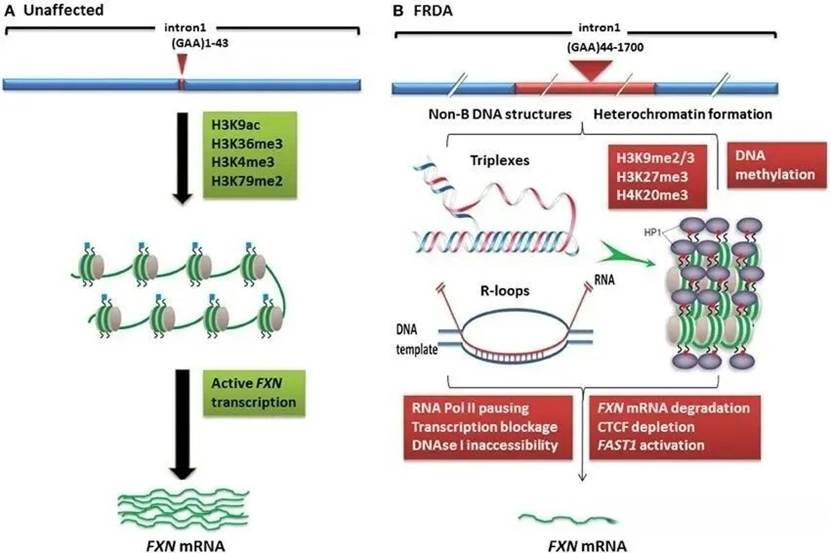
▲ 弗里德赖希共济失调 (FRDA) 中FXN基因沉默模型
FXN基因第一内含子GAA序列的异常扩增会病理性抑制可溶性线粒体蛋白Frataxin的水平,而Frataxin蛋白参与铁硫簇的合成与修复,对线粒体铁代谢和铁稳态至关重要。Frataxin的缺失会直接引发线粒体铁代谢紊乱和氧化应激,进而对高能量需求的组织,特别是小脑齿状核的神经元和心肌细胞,造成不可逆的损伤,因此FA也被归类为线粒体疾病。据统计,大约有65%FA患者会出现心电图异常,主要表现为肥厚型心肌病,这是其常见的并发症和主要死因之一。目前,临床上仅有Biogen公司的一款口服Nrf2激活剂Skyclarys获批上市,用于治疗成人和16岁及以上青少年FA患者,每年费用大约37万美元,尚无针对FA心肌病的有效药物,亟需开发能够从根源上纠正基因缺陷的创新疗法。
LX2006是一种基于重组腺相关病毒 (rAAV) 的基因替代疗法,旨在采用对心脏组织和中枢神经系统表现出极佳组织嗜性和转导效率的AAVrh10载体搭载CGA组成型启动子递送经密码子优化的全长人源Frataxin (FXN) 基因用于治疗弗里德里希共济失调 (FA) 相关心肌病。此前,LX2006已经获得美国FDA授予的再生医学先进疗法资格认定 (RMAT)、孤儿药资格认定 (ODD) 、快速通道资格认定 (FTD) 和儿科罕见疾病资格认定 (RPDD)。
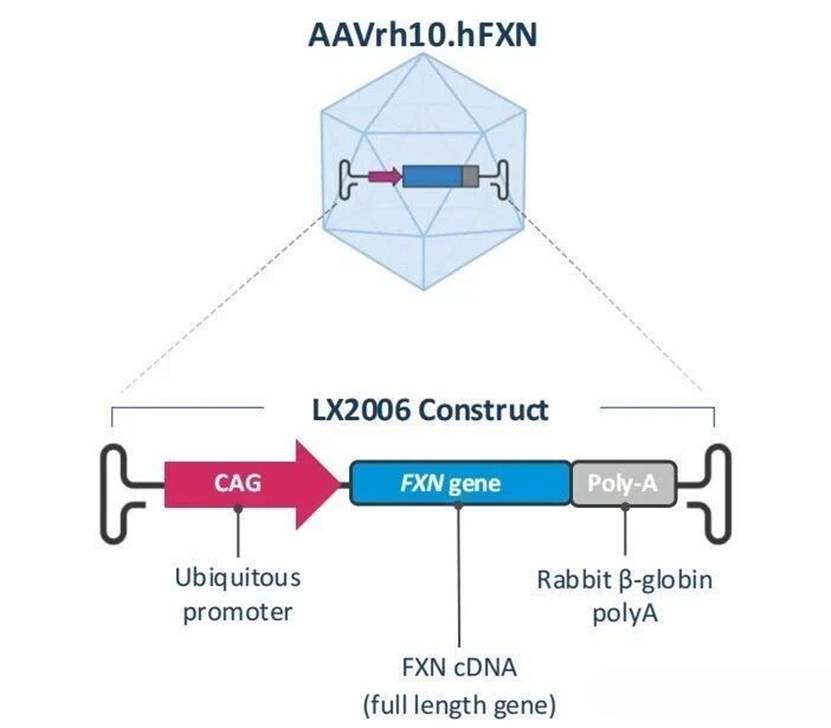
▲ LX2006载体设计
目前心血管领域对FA心肌病的治疗主要依赖传统的β受体阻滞剂或ACEI等抗心衰药物。这些药物仅仅是减轻心脏后负荷,属于治标范畴;而LX2006则是通过基因补偿直接填补了代谢途径中的核心缺失环节,从而在线粒体中重构Frataxin蛋白的表达,从源头切断了心肌肥厚的病理链条。
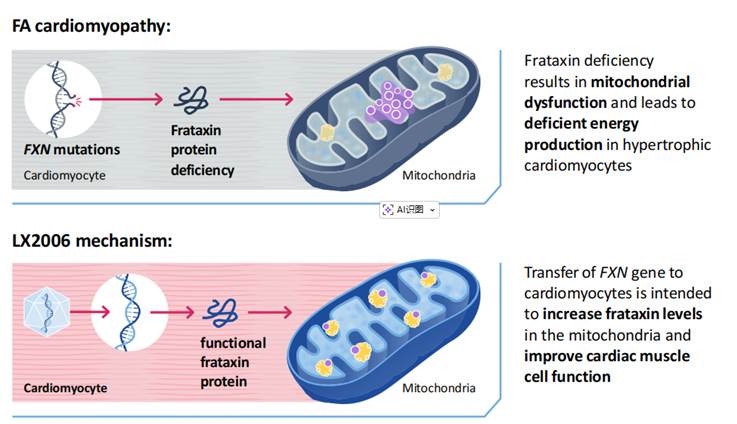
▲ LX2006作用机制
这项首次人体I/II期临床试验共入组了17名患有FA相关心肌病的成年患者,分为三个剂量递增组 (1.8×10¹¹、5.6×10¹¹和 1.2×10¹² vg/kg) 接受单次静脉给药。在随访超过6个月的患者中,LX2006 总体耐受性良好,不良事件大多为轻度且短暂,报告了4例严重不良事件,其中包括1例发生在12个月时的2级心肌炎,该病例被认为可能与治疗相关,并经皮质类固醇治疗后缓解。迄今为止未报告任何3级及以上的严重不良事件。更为关键的是其展现出的生物学活性,核心生物标志物左心室质量指数 (LVMI) 显著下降了-33%;即使是包含低剂量组的整体评估,12个月的LVMI平均降幅也达到了-23%,这直接印证了靶向基因递送成功遏制了心肌肥厚的恶化趋势。
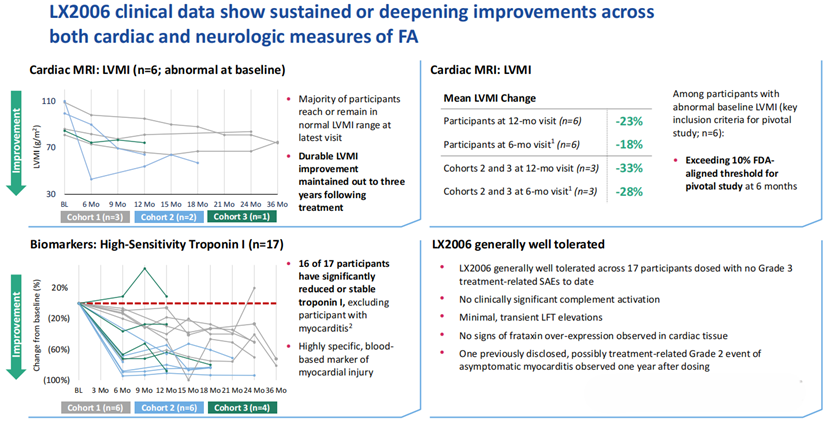
▲ LX2006临床数据
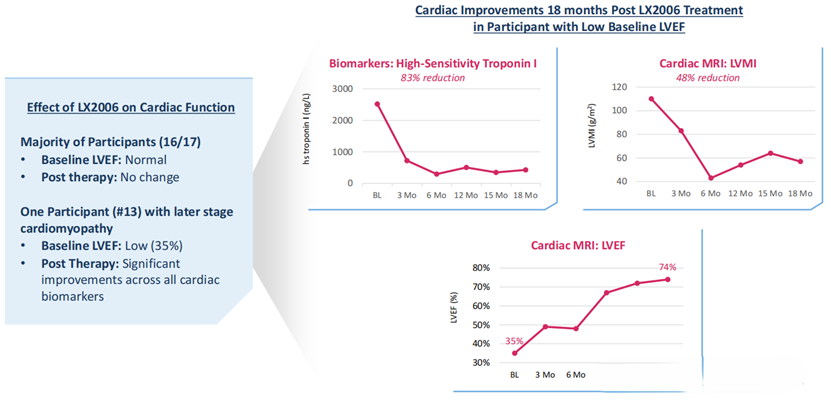
▲ LX2006临床数据
除了作为主要观测终点的心脏指标改善外,研究团队还观察到了患者神经系统功能的意外获益。通过与UNIFAI自然病史研究的倾向性匹配对照组进行对比,接受LX2006治疗的患者在改良版弗里德赖希共济失调评定量表 (mFARS) 的平均得分上取得了具有统计学意义的显著改善 (P=0.03)。这种双重获益机制,极大地拓展了该疗法的潜在市场上限。
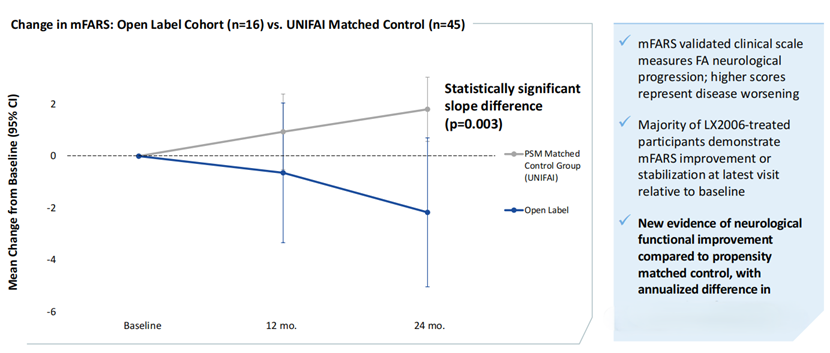
▲ LX2006临床数据
迈向最终确证:SUNRISE-FA II期临床蓄势待发
基于目前积极的临床数据,LX2006已获得美国FDA授予的突破性疗法资格认定 (BTD),这不仅意味着其在审批通道上的全方位提速,更代表着监管机构对FA相关心肌病未满足临床需求的迫切回应。2026年2月,Lexeo已向FDA递交了下一阶段SUNRISE-FA 2关键性临床试验的最终设计方案。该研究将进一步扩大样本量,并听取了FDA关于消除医生选择偏倚的建议,继续以左心室质量指数 (LVMI) 为核心主要终点,主要次要终点包括高敏肌钙蛋白I、左心室壁厚度、mFARS、KCCQ、无事件生存期 (死亡/MACE), 该试验将于2026年上半年正式启动。
除了在分子机制方面得到充分验证之外,在CMC层面Lexeo同样展现出了极强的技术底蕴,提前解决了LX2006商业化规模量产的合规性问题。根据披露的信息,FDA已于2025年11月批准了其生产工艺从HEK293向昆虫细胞-杆状病毒表达系统 (Sf9) 的工艺转移。利用Sf9系统进行AAV生产摆脱了传统质粒转染的局限,不仅实现了超高产率 (1.0E15 vg/L) ,极高的下游回收率 (>55%),更是将空载率严格控制在25%以下,有望大幅降低其生产成本。结合2026年3月FDA在首次CMC开发与准备计划会议上给予的宽容态度 (支持灵活工艺验证) ,LX2006冲刺上市前的工艺路障已被彻底清除。随着2026年SUNRISE-FA II期关键性临床的启动,LX2006极有可能成为定义下一代代谢性心血管病基因疗法的新标杆。
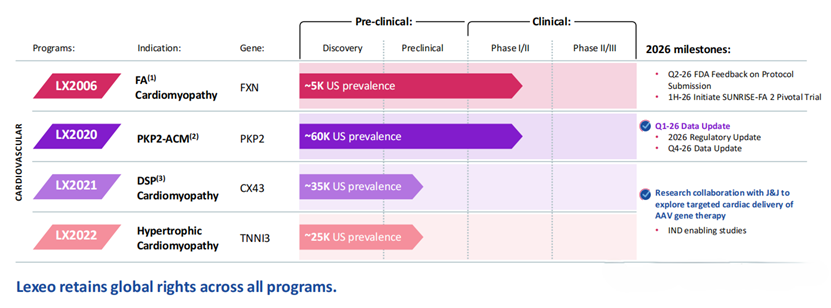
▲ Lexeo Therapeutics公司研发管线布局