4月7日,美国生物技术公司Insmed正式宣布,其核心药物brensocatib(商品名:Brinsupri)治疗中重度化脓性汗腺炎(HS,又称“反常性痤疮”)的2b期CEDAR研究,未能达到预设的主要及次要疗效终点,公司已决定终止该药物在该适应症领域的全部开发计划,给HS这一罕见病的新药探索带来沉重打击。

据悉,CEDAR研究为全球多中心随机双盲安慰剂对照试验,专门针对中重度HS患者设计,共纳入214名受试者,核心目的是评估brensocatib 10毫克、40毫克每日一次给药方案的疗效与安全性。
试验核心数据显示,治疗第16周时,两个剂量组患者的总脓肿和炎性结节计数较基线分别减少45.5%和40.3%,而安慰剂组的降幅高达57.1%,治疗组疗效显著不及安慰剂,未达到任何预设疗效目标。
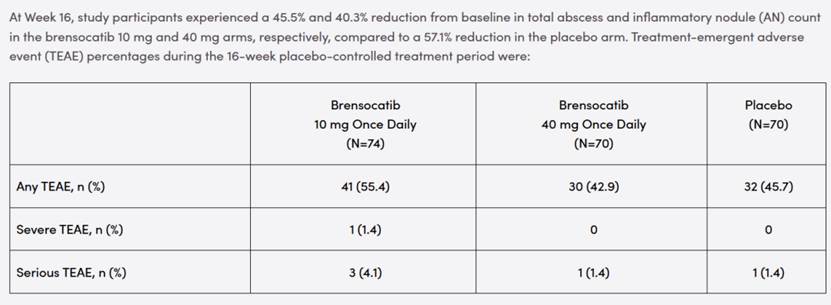
尽管该药物在试验中耐受性良好,未发现新的安全信号,不良事件发生率与安慰剂组无明显差异,但Insmed明确表示,基于CEDAR研究的明确阴性结果,继续推进其在HS领域的开发已无临床和商业价值,因此决定终止相关研发工作。
HS是我国罕见病目录中的慢性炎症性皮肤病,患病率 33.49/10 万,患者多青春期后发病,确诊延迟久、治疗手段匮乏。
此次CEDAR研究的失败,是该药在拓展新适应症道路上遭遇的又一次挫折。
此前在2025年12月,该药物在治疗无鼻息肉的慢性鼻鼻窦炎(CRSsNP)的IIb期BiRCh研究中同样未能达到疗效终点,并导致公司股价在当时出现大幅下跌。
然而,与上次市场剧烈反应不同,此次HS适应症失败的消息公布后,Insmed股价在4月8日保持了相对平稳。市场分析认为,这主要得益于该药作为首个获批治疗非囊性纤维化支气管扩张症(NCFB)的靶向药物,展现出巨大的商业潜力。
该药已于2025年8月在美国获批上市,Insmed预计其2026年全球销售额将至少达到10亿美元,强劲的商业表现为公司提供了坚实的“安全垫”。