做基因治疗、基础科研的小伙伴,是不是总被 AAV 相关问题难住?在看文献的时候也是否会好奇为什么有的使用AAV8,有的使用AAV9或者其他的呢?那么AAV 到底是什么?天然存在的还是人工改造的?”“AAV1、2、5、8、9… 这么多血清型,核心差异有哪些呢?
一.什么是腺相关病毒?
1.AAV的来源:
腺相关病毒于1965科学家在实验室培养腺病毒的时候偶然发现, 它常以 “卫星病毒” 的形式伴随腺病毒存在,无法单独复制,必须依赖腺病毒等辅助病毒才能完成增殖。
天然状态下,AAV 广泛存在于人类和其他灵长类动物体内,肝脏、肌肉、肾脏等组织中都可能检测到它的踪迹。最让研究人员眼前一亮的是天然 AAV 不致病,对人体没有明显危害,这也是它后来成为基因治疗载体的核心前提。
2.AAV的特性、结构和基因组:
①多数 AAV 结构、特性都差不多,只有 AAV5 和其他类型差异最大,并且 AAV 很容易改造,耐酸耐碱耐高温,稳定性强。
②AAV 的核心结构是一条约 4.7kb 的单链 DNA,外面包着一层 20-25nm 的 “外壳”(二十面体衣壳,无包膜)。
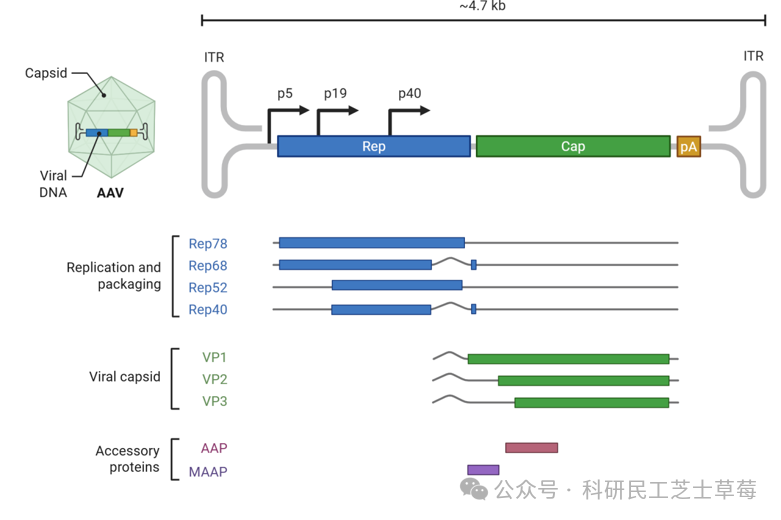
③AAV 基因组以 rep(复制功能)和 cap(衣壳合成)为核心基因,两端辅以反向末端重复序列(ITR)。凭借回文核苷酸序列,ITR 可形成 T 形发夹结构,为病毒基因组复制与包装提供结构基础,同时兼具调控病毒基因表达及介导宿主基因组整合的功能。rep 基因的 ORF 编码基因调控、复制、转录及衣壳化相关的非结构蛋白,cap 基因的 ORF 则编码 VP1、VP2、VP3 三种结构蛋白,三者在 AAV 颗粒中按 1:1:10 的摩尔比组成衣壳。不同 AAV 血清型的组织靶向特异性差异,本质是 cap ORF 的加工方式不同所致,最终体现为免疫特性与转导效果的分化。
3.AAV病毒的使用:
在基因工程改造后,科研人员会去掉 AAV 的 rep 和 cap 等病毒自身基因,插入目的基因(比如治疗性基因、报告基因)。改造后的 AAV 能够把目的基因精准送到目标细胞 / 组织中,且不会整合到宿主基因组(少数血清型除外),安全性高。
二.AAV血清型是什么?
不同血清型核心区别在于病毒表面的衣壳蛋白(由 cap 基因编码) 不同。衣壳蛋白是 AAV 与宿主细胞表面受体结合的关键,决定了病毒能精准到达哪些组织(靶向性)、感染效率有多高(递送能力),以及能否穿过特殊屏障(如血脑屏障)等。
总之血清型直接决定 AAV 的靶向特异性、感染效率、组织穿透能力和免疫原性,选对血清型,是基因递送实验成功的第一步!目前已发现的 AAV 血清型有数十种,其中 AAV1-13 是科研和临床中最常用的天然血清型,除此之外人工改造的多种血清型。
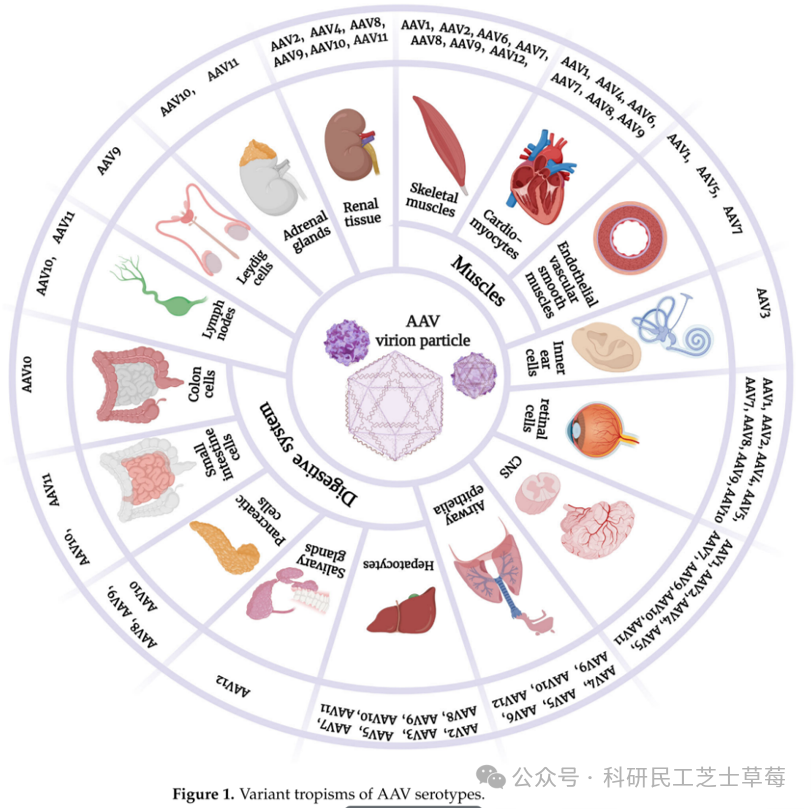
三.各种 AAV 血清型的简洁介绍
1.AAV1:AAV1 它并非直接从生物组织中分离得到,而是最初作为腺病毒(Ad)制剂的污染物被发现的。在受体结合方面,AAV1 以唾液酸作为主要细胞表面受体,同时依赖 AAV 受体(AAVR)作为辅助受体。由于其衣壳缺少肝素结合所需的 R585、R588 氨基酸残基,因此无法与肝素结合,不能通过肝素柱进行纯化;衣壳无翻译后修饰(PTM)作为首个获批用于基因治疗的病毒载体,AAV1 的转导特性在 1999 年被明确:其对骨骼肌的转导效率在当时研究的载体中是最高的。后续研究进一步证实,AAV1 对鼠、犬、NHP 的骨骼肌具有显著的靶向性;同时它也能有效转导小鼠大脑中的神经元、神经胶质细胞、室管膜细胞,以及心脏、血管内皮 / 平滑肌和视网膜。
2.AAV2:AAV2病毒于1965 年首次发现(猿猴 Ad 制剂污染物),是研究最透彻的血清型;以硫酸乙酰肝素蛋白聚糖(HSPG)为主要受体,需 FGFR1、整合素等共受体辅助进入细胞;衣壳有泛素化、磷酸化等多种 PTM;可通过肝素柱纯化,靶向肾、肝、视网膜、中枢非分裂细胞等多组织。
3. AAV3:AAV3从人类组织分离,受体同 AAV2(HSPG),需人肝细胞生长因子受体(hHGFR)辅助;衣壳有乙酰化、糖基化等 PTM;曾因体外转导效率低被忽视,后发现对人类肝癌细胞、NHP 肝细胞转导极高效,也能靶向小鼠耳蜗内毛细胞,需衣壳修饰优化效率。
4. AAV4:AAV4起源于非洲绿猴(NHP),抗原性独特;以 α-2,3-O - 连接唾液酸为受体,可通过粘蛋白柱(结合唾液酸)或离子交换层析纯化;衣壳仅泛素化 PTM;主要靶向中枢室管膜细胞,视网膜下递送可稳定转导视网膜色素上皮(RPE)细胞,也能转导小鼠肾、肺、心脏细胞。
5. AAV5:AAV5于1983 年从人类生殖器病变中分离(唯一直接来自人体组织的血清型),遗传差异最大;以唾液酸 + 血小板衍生生长因子受体(PDGFR)为受体;衣壳有泛素化、糖基化等多种 PTM;可转导 AAV2 无法感染的细胞,靶向小鼠视网膜感光细胞、气道上皮、脑内多种神经元,也能转导肝细胞。
6. AAV6:AAV6是 AAV1 和 AAV2 的天然杂交体(基因组同源性高),以唾液酸 + HSPG 为受体,EGFR 为共受体;衣壳仅乙酰化 PTM;可通过肝素 / 粘蛋白柱纯化;对小鼠、犬的气道上皮、骨骼肌转导效率优于 AAV2,也能靶向猪、羊等的心肌细胞。
7.AAV7:AAV7于2002 年从恒河猴(NHP)分离,受体机制未知,不结合肝素;衣壳有糖基化、磷酸化等多种 PTM;人类体内抗体阳性率低(临床优势);对小鼠骨骼肌转导效率与 AAV1 相当,也能靶向肝、NHP 脑皮质及脊髓,可转导视网膜感光细胞。
8. AAV8:AAV8于2002 年从恒河猴分离,以层粘连蛋白受体(LR)为主要受体;衣壳有磷酸化、糖基化等 PTM;可通过双离子交换层析或碘克沙醇纯化;肝转导效率在鼠、犬、NHP 中均远超其他血清型,能穿透血管屏障靶向骨骼肌、心肌,局部递送可转导胰腺、肾细胞,也能转导视网膜多种细胞。
9. AAV9:AAV9于2004 年从人类分离,以末端 N - 连接半乳糖为受体;衣壳 PTM 最丰富(泛素化、糖基化等);可通过离子交换层析或蔗糖梯度纯化;能高效穿过血脑屏障,靶向中枢神经元、星形胶质细胞,全身递送后转导效率优于其他血清型,对心肌、肝、视网膜等多组织均有高趋向性。
10. AAV10/11:2004 年从食蟹猴(NHP)分离,衣壳分别与 AAV8、AAV4 相似;无 AAV2 交叉抗体(适合 AAV2 抗体阳性人群);受体未知,常用碘克沙醇纯化;AAV10 靶向 NHP 肠、肝及小鼠视网膜多种细胞,AAV11 轻微靶向 NHP 中枢及小鼠神经元、星形胶质细胞。
11. AAV12:AAV12是从猿猴 Ad 种群分离,血清学特性独特;不依赖 HSPG / 唾液酸,可能以甘露糖为受体成分;可通过 AVB 琼脂糖纯化;人类抗体中和抗性强;靶向小鼠唾液腺、肌肉,鼻内给药可转导鼻上皮。
12. AAV13:AAV13从猿猴 Ad 分离,可结合 HSPG,结构与 AAV2/3 相似;衣壳保留 AAV 核心特征,但趋向性、转导效率相关数据仍有限。
除天然血清型外,通过 “嵌合”(衣壳整合不同血清型亚基)、“DNA 改组”(重组不同血清型基因组)、“易错 PCR” 等工程策略,构建出镶嵌、嵌合、组合文库类载体,可增强转导效率、降低免疫原性,或实现特定细胞的精准靶向。
参考:
Issa SS, Shaimardanova AA, Solovyeva VV, Rizvanov AA. Various AAV Serotypes and Their Applications in Gene Therapy: An Overview. Cells. 2023 Mar 1;12(5):785.
Suarez-Amaran L, Song L, Tretiakova AP, Mikhail SA, Samulski RJ. AAV vector development, back to the future. Mol Ther. 2025 May 7;33(5):1903-1936.