导语
2025年7月12-13日,蔻德罕见病中心与瑞鸥公益基金会在杭州联合主办患者社群推动药物研发赋能会暨全国罕见病患者组织网络年会。
会议以 “患者社群推动自救式药物研发” 为核心,形式与内容有新突破。围绕药物研发全流程设四大主题分享,邀多领域专家参与,通过四个工作坊促进患者与专家深度交流,旨在解决各阶段核心问题,沉淀经验、形成共识、助力行动。
此次赋能会吸引66个疾病的120位代表,含39个患者组织代表。会上特设 “微光博物馆”,参会者的信物成为情感桥梁与对话媒介,传递个体故事的温度与力量。
蔻德罕见病中心将通过连载发布本次赋能会的相关内容,本篇为系列内容16。
林念炜《国外患者组织推动的个体化治疗:从自救到变革的机遇与挑战—— 技术突破、协作模式与未解难题》

瑞鸥公益基金会首席科学官林念炜博士分享的主题是《国外患者组织推动的个体化治疗:从自救到变革的机遇与挑战—— 技术突破、协作模式与未解难题》
在全球 7000 多种罕见病中,95% 尚无有效治疗方案,药企因患者基数小、研发成本高而动力不足。在此背景下,患者组织正成为推动个性化治疗的核心力量。林念炜博士通过多个亲身经历的案例,揭示了国外患者如何从 “被动等待” 转向 “主动创造”,构建起从研发到可及的完整生态。
一患者驱动的两种核心模式
国外患者推动个性化治疗主要形成两类成熟模式,各有侧重却殊途同归。

家庭主导模式以 “小而精” 的单点突破见长。2016 年,3 岁女孩 Mila 被确诊为 CLN7 巴顿病(一种罕见神经元蜡样脂褐质沉积症),表现为失明、癫痫频发及运动功能丧失,预期寿命仅 8-12 岁。其母亲 Julia Vitarello 通过社交媒体联系到波士顿儿童医院 Timothy Yu 团队,创立 “米拉奇迹基金会” 筹资 300 万美元,仅用 10 个月就完成反义寡核苷酸(ASO)药物 Milasen 的研发。该药物通过修复基因剪切缺陷,使 Mila 的癫痫发作减少 70%,吞咽功能显著改善,成为全球首个 “N-of-1”(单患者定制)ASO 疗法案例,直接推动 FDA 建立个体化药物快速监管框架。
社群协作模式则追求 “大而全” 的平台化突破。n-Lorem 基金会由 Ionis 制药创始人 Stanley Crooke 创立,专为患者数≤30 人的超罕见病提供免费 ASO 药物及终身治疗。截至 2025 年,该基金会已为 100 余例患者开发药物,其中针对未知罕见癫痫基因突变的幼儿,15 个月内完成药物交付,显著降低癫痫发作频率。其核心在于整合科研资源、共享技术经验,将单例 ASO 研发成本从 200 万美元降至 50-150 万美元。
二技术突破与案例实践
个性化治疗的技术路径已形成多元布局,各有其适用场景与突破。

ASO 疗法以开发周期短(8-12 个月)、非整合性(无基因组改变风险)成为快速干预首选。除 Mila 案例外,2024 年,Timothy Yu 团队为 TNPO2 基因突变的新生儿 Leo 开发的 ASO 药物,8 个月内完成设计与给药,使患儿发育商(DQ)从 35 提升至 65,实现从 “无法抓握” 到 “支撑坐立” 的功能逆转,首次证实 ASO 可修复发育基因缺陷。
AAV 基因替代疗法以长效性(单次治疗持续数年)见长。7 岁男孩 Michael 患 SPG50(全球仅 80 例),因 AP4M1 基因突变导致进行性四肢瘫痪与癫痫。其父亲 Terry Pirovolakis 创立 CureSPG50 基金会,筹资 300 万美元联合加拿大多伦多病童医院团队,通过脑脊液注射高剂量 AAV 载体(1×10¹⁵ vg),12 个月内使 Michael 从 “仅能爬行” 恢复至 “辅助行走”,癫痫完全消失,成为首例单患者 AAV 临床试验成功案例。
CRISPR 碱基编辑则实现 “永久修复”。2025 年,全球首例 CPS1 缺乏症新生儿接受碱基编辑治疗,6 个月内完成从设计到给药,为新生儿急症提供 “速效救治” 模板,但脱靶风险与伦理争议仍待解决。
三融资与生态:钱从哪里来?
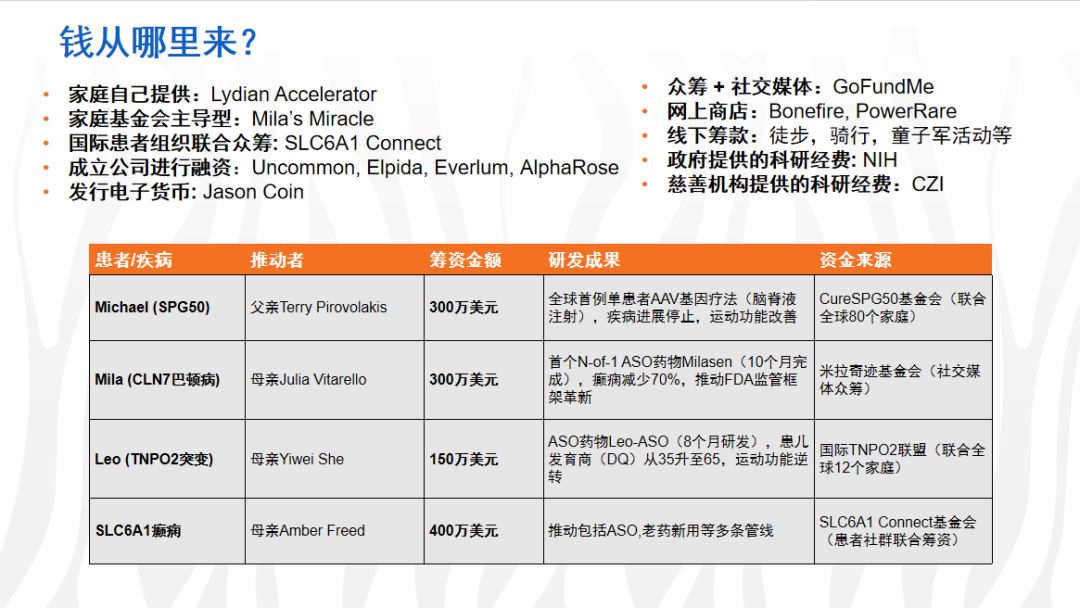
资金难题的破解是患者推动治疗的关键。国外已形成多元筹资体系:
家庭与社群自筹:SLC6A1 癫痫患者母亲 Amber Freed 联合全球家庭众筹 400 万美元,推动 ASO 及老药新用管线;Michael 家庭通过基金会整合 80 个家庭资源,募集 300 万美元。
创新融资工具:优先审评券(PRV)成为重要激励,药企若推动罕见病治疗至临床,可获 FDA 快速审批资格,该资格最高可售 3.5 亿美元。Elpida 公司计划通过推动 5 个罕见病药物研发,获取 2 张 PRV 券以反哺更多项目。
跨界资整合:线上通过 GoFundMe 众筹、PowerRare 公益商店(销售定制商品)募集资金;线下通过徒步、骑行等活动扩大社会影响力,如西班牙渐冻症患者组织骑行 400 英里穿越死亡谷,联动全球患者社群。
公益与政府支持:扎克伯格基金会(CZI)每年资助 5-6 例患者,每例 20 万美元启动研发;美国 NIH 为个性化治疗提供专项科研经费。
四挑战与启示
尽管进展显著,个性化治疗仍面临多重挑战:成本高昂(AAV 疗法 200-350 万美元 / 例,ASO 50-200 万美元 / 例)、医保覆盖缺失导致可及性不公;高剂量 AAV 引发免疫风暴的安全性风险,以及长期疗效数据缺失等。
但这些案例揭示核心启示:患者的主动性是打破困局的关键。从 Mila 母亲的社交媒体求助,到 Michael 父亲的全球筹资,再到蔡磊推动中国渐冻症研究(建立 iPSC 筛选平台、募集超 100 条管线),都证明 “唯有发声,才能被看见”。
正如 Michael 父亲所言:“直到时间尽头,我们也要找到拯救的方法。” 这种坚韧正在重塑罕见病治疗的生态,为更多 “小众” 疾病带来希望。
蔻德罕见病中心&瑞鸥公益基金会将持续关注和参与推动罕见病患者社群推动药物研发这一议题的工作。如您对这一议题有兴趣,希望参与交流、进行项目合作、提供其他支持等,都可以与我们取得联系,请您留下基础信息,我们会及时与您取得联系,共同为罕见病患者社群早日实现有药可医而努力!

