罕见病信息网隆重推出《壹周罕见药闻》这一独具特色的品牌栏目。该栏目在每周日更新,以呈现当周罕见病领域的最新消息和下周的罕见病活动预告。我们以更高端、更权威的视角,为您剖析最新、最热门的罕见病信息。
罕药快讯
01 针对亨特综合症生物制品许可,美国优先审评释放积极信号
02 挚盟医药“渐冻症”在研新药在中国获批2/3期临床研究
7月9日,上海挚盟医药科技有限公司宣布:公司自主研发的针对中枢神经系统疾病的新一代KCNQ2/3钾离子通道开放剂CB03-154近日获得中国国家药监局药品审评中心(CDE)的临床试验批准,即将在中国开展针对肌萎缩侧索硬化(又称“渐冻症”,ALS)的临床2/3期研究。此前,CB03-154片已获得美国FDA授予的孤儿药资格(Orphan Drug Designation, ODD),开发用于ALS患者的治疗。
ALS是一种严重的神经系统退行性疾病,可造成大脑和脊髓神经细胞的功能紊乱、丧失甚至凋亡,最终导致肌肉失去控制。ALS的初始症状通常包括手臂或腿部肌肉抽搐和无力、吞咽困难或言语不清。
03 Taiho DMD 药物候选物 TAS-205 三期试验失败,未达主要终点
Taiho Pharmaceutical公司用于治疗杜氏肌营养不良症(DMD)的研究性治疗未能在功能性运动测试结果中显示显著改善,未能达到3期临床试验的主要终点。这项名为REACH-DMD的研究在日本进行,涉及82名5岁及以上的DMD男性患者。
Taiho Pharmaceutical,Otsuka Holdings的子公司,尚未披露在这次挫折后对TAS-205的未来计划。该公司表示,REACH-DMD研究的进一步发现预计将在即将举行的学术会议上公布。
04 重大进展!罕见病药物获美国突破性疗法认定
7月7日,Lexeo Therapeutics宣布,美国食品药品监督管理局(FDA)已授予LX2006突破性疗法认定,这无疑为众多心血管疾病患者带来了新的希望。
FA心肌病是一种由frataxin基因功能丧失突变引起的罕见、进展性疾病。
05 股价大涨180%!CAR-T细胞疗法获FDA孤儿药资格认定
06 全球首款!罕见病口服急救药获批!
07 打破垄断,填补空白!两款国产罕见病疗法同日迎新进展
近日,两款国产罕见病疗法相继取得关键进展,惠及罕见病患者群体。正大天晴的国产首仿重组人凝血因子VIIa正式获批,将提升血友病患者的治疗可及性。
同时,石药集团针对罕见病甲基丙二酸血症(MMA)的高浓度盐酸羟钴胺注射液获准开展临床试验,有望填补全球该适应症治疗药物的空白。
罕圈动态
01 突破AAV载体瓶颈,国内基因治疗又一最新突破性成果发表
鼐济医药与中南大学湘雅医院彭镜教授团队合作于近期在Molecular Therapy期刊上发表题为Gene Therapy with covalently-closed-end AAV vector for Spinal Muscular Atrophy的研究论文,公开基于共价闭合末端AAV(cceAAV)技术平台开发的候选药物NKG001的临床试验数据,验证了其在两例12–24个月SMA患儿中的快速、安全且有效的治疗表现。
02 美佛州立法破局罕见病,斥资千万美元攻坚罕见病,奠基千亿基因产业
03 国家医保局:罕见病药可纳入商保目录,你期待哪种药入选?
7月10日,国家医保局正式发布2025年国家基本医疗保险及商业健康保险创新药品目录调整工作方案系列文件,7月11日—20日在国家医保服务平台开通网上申报系统。
这将是国内第一版商保创新药品目录,主要纳入超出保基本定位、暂时无法纳入基本目录,但创新程度高、临床价值大、患者获益显著的创新药,推荐商业健康保险、医疗互助等多层次医疗保障体系参考使用。
04 国家发布86个罕见病病种诊疗指南(2025年版)
7月10日,为进一步提高罕见病诊疗规范化水平,保障医疗质量安全,国家卫健委组织对《第二批罕见病目录》中软骨发育不全等86个病种分别制定了诊疗指南(见附件,可在国家卫生健康委网站医政司栏目下载)。
05 59.23亿!阿斯利康获AAV基因治疗技术,加码罕见病
06 上市时间缩短到1到2个月,FDA推出优先审批计划以加速罕见病药物开发
07 诺奖得主、基因编辑女皇押注CRISPR治疗儿童罕见病
近日,加州大学旧金山分校宣布成立儿科CRISPR基因编辑治疗中心,专注于利用基因编辑技术为儿童罕见遗传病提供突破性基因编辑疗法。该治疗中心由诺贝尔奖得主、CRISPR技术顶级权威专家詹妮弗·杜德纳教授与陈-扎克伯格倡议联合创始人普莉希拉·陈合作发起,并且率先获得了2000万美元研究经费资助。
目前,全球约有6000种罕见遗传疾病,至少影响超过3亿患者,其中大多数患者为儿童。CRISPR的精准基因编辑能力,为这些患儿和家庭带来了前所未有的希望,也预示着罕见疾病治疗将迎来新纪元——基因编辑疗法的全面应用。
08 默克以34亿美元完成对SpringWorks的收购
在获得监管部门批准并满足惯例成交条件后,默克化工完成了此前宣布的对SpringWorks Therapeutics的收购,企业价值为30亿欧元(34亿美元)。
默克通过并购 SpringWorks 获得两项针对治疗方案有限的罕见肿瘤的产品,其中 Ogsiveo(nirogacestat)已获美国 FDA 批准,且于 2025 年 6 月获得欧洲 EMA 人用医药产品委员会(CHMP)建议批准,用于需要全身治疗的进展期类风湿瘤成人患者,另一项产品具体名称未提及。
09 NIH终止资助动物实验,重点加注类器官!
7月7日,美国国立卫生研究院(NIH)在与美国食品药品监督管理局(FDA)联合举办的研讨会上宣布了一项历史性决策:不再资助仅依赖动物试验的新研究项目,所有新的NIH资助机会都应纳入新方法(NAMs)的考量。这一决策标志着跨越近一个世纪的动物试验主导时代迎来终结。
NIH负责项目协调、规划与战略事务的副主任Nicole Kleinstreuer博士着重强调,所谓的“新方法”(NAMs),指从计算机建模、人工智能,到器官芯片与类器官技术等前沿动物替代技术。未来,NIH的自主机会将会向相关领域着重偏移。
活动预告
01 2025第十四届中国罕见病高峰论坛报名通道开启 | 汉卫罕见 共筑希望

02 你的研究需要被看见!中国罕见病高峰论坛壁报征集启动
2025第十四届中国罕见病高峰论坛将于2025年9月19日-21日由蔻德罕见病中心联合华中科技大学同济医学院附属同济医院在武汉共同举办。
03 志愿者招募 | 中国罕见病高峰论坛,期待你的力量!
04 报名通道开启 | 首届家族性高胆固醇血症(FH)大会暨患友交流会
05 追光之旅-儿童罕见骨病多学科诊疗学术论坛鲁豫地区专场线上会直播预告
论坛的核心目标之一,就是将顶尖专家的知识和经验,直接传递给需要的患者和家庭!
时间:2025年7月15日(星期二)晚上 19:30 - 22:00
06 2025华西国际罕见病学术论坛——“会议征文” & “科普作品”!火热报名中~

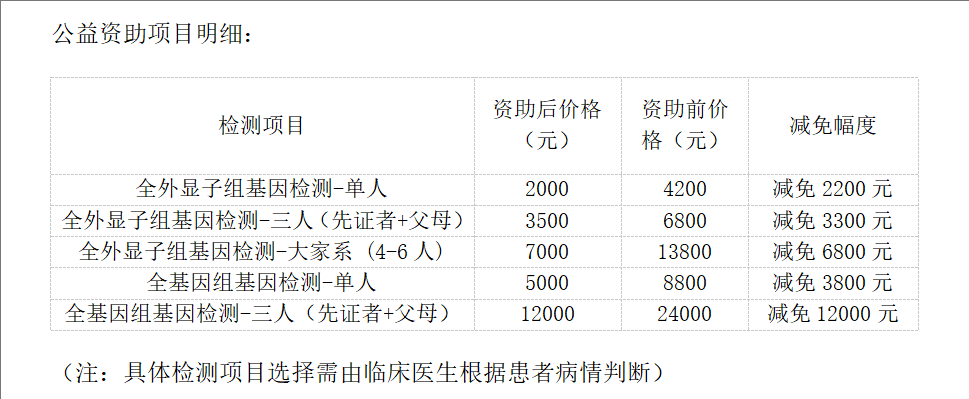
07 “冀罕守护”为罕见病家庭减免千元基因检测费
全球已知罕见病超7000种,我国患者超2000万。 在河北这片7400万人生活的土地上,预估有数十万罕见病患者在苦苦求医。约80%的罕见病由遗传缺陷导致,基因检测是确诊的“金标准”,但动辄数千元的费用,曾让多少家庭望而却步,延误诊断与治疗?
为打破这一困境,由河北省药学会罕见病专委会联合石家庄金域医学发起的“冀罕守护”罕见病基因检测公益项目,于6月28日在河北省药学会罕见病专委会第八次学术年会上正式启航!
如何申请?两步轻松搞定!
家有疑似或确诊罕见病患者,正为基因检测费用发愁?“冀罕守护”助您一臂之力!申请流程便捷:
1.线上申请:
关注“燕赵罕见病” 官方微信公众号。
→在公众号内找到公益项目申请入口(菜单栏)
→在线填写并提交申请表单。
2.流程协助:
提交申请后,项目组工作人员将主动联系您,指导您完成后续所需的材料准备、样本采集等流程。
在工作人员的专业协助下,轻松走完“冀罕守护”公益项目的剩余步骤。
08 2025年中国罕见病大会,报名进行中
由全国罕见病诊疗协作网办公室、中国罕见病联盟等携手多方主办的2025年中国罕见病大会,将于9月19日-25日举办(其中线下会议9月19日-21日在北京召开),期待您点击上图报名大会,与海内外上千位专家,共商罕见病事业发展新格局。
罕见同心,聚力同行,我们诚挚邀请关心罕见病群体的公立医疗机构、高等院校、患者组织等成为2025年中国罕见病大会的协办单位,如您有意向可扫描下方二维码申请,截止时间为8月15日,主办方将于8月30日前完成审核和联络。期待您的加入,与我们共建罕见生命的美好明天!
