非典型溶血性尿毒症综合征(aHUS)更名为补体介导的血栓性微血管病(CM-TMA),这一命名变更反映了对这组罕见危重疾病认识的深化。CM-TMA以微血管病性溶血性贫血、血小板减少症和多器官损伤为特征,其本质是替代补体通路失调所致,常由遗传变异或自身抗体触发。
本文结合2025年3月27日新发布的一篇综述,探讨CM-TMA的命名演变、病因、临床表现、诊断路径以及妊娠相关情况,为大家提供认识与诊断这一复杂疾病的关键要点。

01
血栓性微血管病(TMA)是一组以微血管病性溶血性贫血、血小板减少和多系统器官损伤为特征的临床疾病。它包括多种实体,如血栓性血小板减少性紫癜(TTP)、继发于感染的溶血性尿毒症综合征(通常与产志贺毒素大肠杆菌[STEC]感染相关),以及非典型HUS,现在称为补体介导的血栓性微血管病(CM-TMA)。
溶血性尿毒症综合征(HUS)传统上分为两类:
第一类是“典型”HUS或STEC-HUS,主要影响5岁以下儿童,通常表现为接触STEC后首日的血性腹泻。志贺毒素导致内皮损伤,引发血栓性微血管病表现。约5%的病例与侵袭性肺炎链球菌疾病相关。
第二类,即CM-TMA(前称非典型HUS),最初指不是由腹泻前驱的TMA表现,通常发生在年龄较大的患者(青少年或年轻成人)。后来确认为一种由替代补体通路不受控制激活介导的疾病,导致形成膜攻击复合物(C5b-9)损伤血管内皮。
随着对替代补体通路功能障碍机制理解的加深,需要更精确的术语。新的专家共识强调将非典型HUS重命名为CM-TMA的重要性,以特指补体功能障碍是主要致病因素的TMA形式。这一更新的命名法有望优化临床研究和治疗管理,允许更有针对性的方法,特别是使用C5抑制剂。
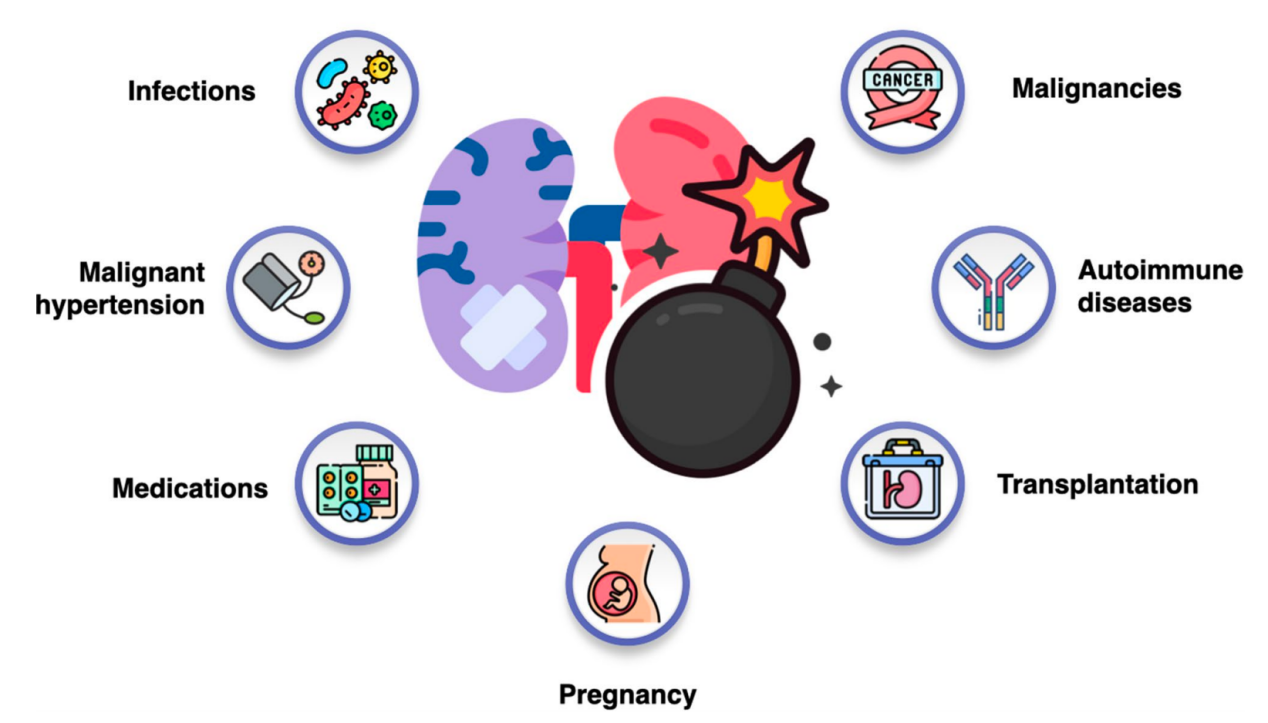
图1:血栓性微血管病的继发性原因
02
CM-TMA特异性源于替代补体通路的失调,继发于补体相关基因的致病变异或补体因子H的自身抗体存在。这种疾病通常由环境因素触发。
补体因子基因的致病变异可导致调节蛋白功能丧失(如因子H、因子I、CD46等)或功能获得性变异(如C3或因子B)。因子H变异最为常见,发生在20%-30%的病例中,并携带最高的复发风险。MCP/CD46变异第二常见(10%-15%),与中等复发风险相关。此外,因子I、C3和因子B变异分别占4%-8%、2%-10%和1%-2%的病例。
约6%的CM-TMA继发于抗因子H自身抗体的存在,大多见于儿科人群(高达25%的病例)。其发展与补体因子H相关蛋白1和3(CFHR1-3)的缺失有关,尽管潜在机制仍不清楚。初始治疗包括治疗性血浆置换,随后是免疫抑制治疗以抑制抗体产生。
03
CM-TMA表现为血栓性微血管病的三个典型特征:微血管病性溶血性贫血、血小板减少和器官损伤,具有某些特定特征。这些临床表现通常发展迅速,如不充分治疗,可能进展至器官衰竭和死亡。
微血管病性溶血性贫血是TMA的标志,特征为红细胞在微循环中由于内皮损伤而破坏。它由以下实验室发现识别:乳酸脱氢酶(LDH)、间接胆红素、网织红细胞计数和游离血红蛋白升高;触珠蛋白降低;以及外周血涂片上存在碎裂红细胞。直接Coombs试验为阴性,除非在继发于肺炎链球菌感染的TMA中,高达90%的病例可能呈阳性。
血小板减少定义为血小板计数低于150,000/mm³或从基线水平下降25%。这种减少是由于血小板在小血管内形成的微血栓中消耗所致。CM-TMA中的血小板减少症严重程度通常比TTP轻。
器官损伤是多系统性的。肾脏受累,特征为肾小球毛细血管内微血栓形成,影响肾小球滤过,是CM-TMA的特征。约50%-60%的患者需要肾脏替代治疗,并且恶性高血压经常被观察到。神经系统表现包括脑病、局灶性缺损、癫痫发作和昏迷,但比TTP明显少见。值得注意的是,约25%的CM-TMA患者可能表现为仅限肾脏的TMA,需要肾活检进行早期检测。
04
CM-TMA的诊断是在疾病急性期除外TTP和TMA继发性原因的一种排除性诊断。需要注意,C3水平在少于50%的患者中降低。
血栓性血小板减少性紫癜(TTP)诊断的金标准是测量von Willebrand因子裂解酶(ADAMTS13)的活性。然而,临床上常使用法国评分和PLASMIC评分等预测工具评估TTP的可能性。在中间或高风险病例(PLASMIC评分≥5)中,建议开始使用新鲜冻结血浆治疗,理想情况下作为治疗性血浆置换(TPE)。ADAMTS13活性水平≥10%,加上没有抗ADAMTS13抑制剂(自身抗体),可排除TTP。
识别TMA的继发性原因对管理这些患者至关重要。研究表明,高达94%的TMA病例有可识别的继发性原因。各种潜在条件可能触发TMA,包括感染、恶性高血压、自身免疫疾病、恶性肿瘤、药物、实体器官和造血干细胞移植,以及妊娠并发症。
STEC-HUS是儿科患者的主要鉴别诊断,诊断基于临床线索(通常在暴露于STEC后约三天发展出的出血性腹泻)、TMA的实验室特征和确认感染的粪便检测。恶性高血压和TMA有复杂的相互关系,其中每一个都可以作为另一个的原因和结果。继发于恶性高血压的TMA表现会随着积极的血压控制而缓解,若不缓解,则应考虑CM-TMA。TMA也可以在实体器官移植和造血移植受者中发生,有多种可能原因。
05
妊娠期最常见的TMA是HELLP综合征(溶血、肝酶升高和血小板减少),通常在先兆子痫存在的情况下发生,治疗涉及终止妊娠。妊娠似乎对CM-TMA有保护作用,可能是因为胎盘依赖CD59和衰减因子(DAF)来调节替代补体通路。然而,在产后期,随着胎盘排出,这种保护消失,CM-TMA发作的风险增加。
如果终止妊娠后,溶血表现仍持续并发展为进行性急性肾损伤,应怀疑CM-TMA。研究表明,血清肌酐≥1.9 mg/dL和LDH≥600 U/dL的组合对诊断产后CM-TMA有极高的特异性和敏感性。在产后48-72小时内未改善的病例中,早期使用C5补体抑制剂是有指征的。
06
总之,补体介导的血栓性微血管病是一组由替代补体通路失调引起的复杂疾病,表现为微血管病性溶血性贫血、血小板减少和器官损伤。其命名从非典型溶血性尿毒症综合征演变为现在的术语,更准确地反映了基础病理生理机制。了解其病因、临床表现、诊断路径以及妊娠相关特点对于早期识别和干预至关重要。CM-TMA的诊断是排除性的,需要排除TTP和继发性TMA原因,而遗传检测则有助于确认诊断和指导治疗。对我们师来说,熟悉这些概念是制定个体化治疗方案的基础,有助于改善这一罕见但严重疾病的预后。
参考文献:
Musalem P. Ten tips for managing complement-mediated thrombotic microangiopathies (formerly atypical hemolytic uremic syndrome): narrative review. BMC Nephrol. 2025;26:158.