3月19日,Immunovant宣布了一项重大战略调整:尽管其核心产品巴托利单抗(batoclimab)在治疗重症肌无力和CIDP的临床试验中达到主要终点,但公司决定暂不向监管机构提交该适应症的上市申请,转而优先推进其新一代FcRn抗体IMVT-1402的开发。这一决策引发了行业对罕见病药物研发策略与市场竞争格局的广泛关注。


巴托利单抗是一款靶向新生儿Fc受体(FcRn)的单抗药物,通过降低致病性免疫球蛋白G(IgG)水平治疗自身免疫性疾病。
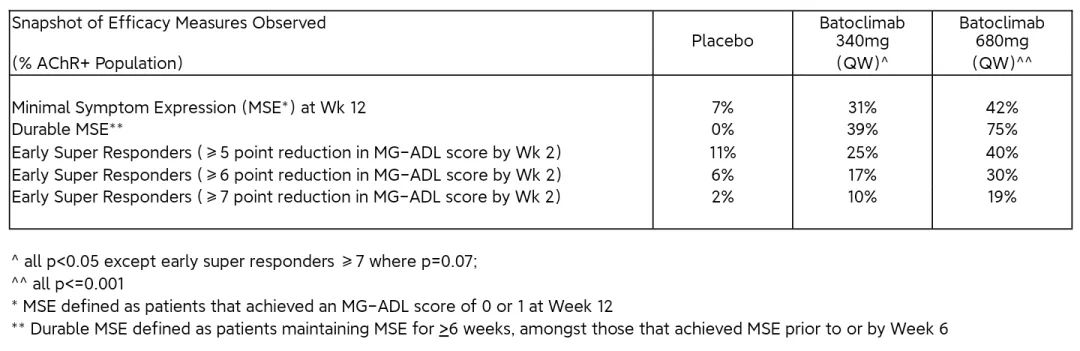
今天刚刚公布的II期临床试验数据显示,在重症肌无力(MG)的关键研究中,乙酰胆碱受体(AChR)阳性人群在 12 周时达到了主要终点,即重症肌无力日常生活活动能力量表(MG-ADL)基线变化。高剂量组(平均 IgG 水平降低 74%)改善了 5.6 分,低剂量组(平均 IgG 水平降低 64%)改善了 4.7 分。
然而,Immunovant在评估后认为,尽管巴托利单抗表现优异,但其潜在的胆固醇升高副作用可能限制长期临床应用。
相比之下,新一代候选药物IMVT-1402在I期临床试验中展现出更优的安全性——在显著降低IgG的同时,未观察到血清白蛋白下降或低密度脂蛋白胆固醇(LDL-C)升高的风险,且皮下注射便捷性突出。这一差异化优势促使公司调整资源分配,聚焦IMVT-1402的多适应症开发。
02 IMVT-1402:同类最优潜力的核心驱动力

IMVT-1402作为改良型FcRn抗体,通过特异性阻断IgG与FcRn的结合,减少对白蛋白代谢的干扰。其I期数据显示,单次给药后IgG降低幅度达63%,且不良事件均为轻中度。此外,该药采用预充式注射器,仅需数秒完成给药。
Immunovant计划于2024年下半年启动IMVT-1402在重症肌无力、慢性炎症性脱髓鞘性多神经病(CIDP)等适应症的注册性临床试验,并利用优先审评凭证加速监管流程。
国内石药集团已从和铂医药引进获得巴托利单抗中国权益,协议总金额超10亿元。
03 结束语
Immunovant的决策折射出行业趋势:在快速迭代的技术背景下,企业需权衡短期收益与长期竞争力。放弃成熟产品的监管申请虽显激进,但集中资源开发更具差异化的管线,或为在激烈市场中脱颖而出的关键。IMVT-1402的潜在优势若获验证,将提供更安全持久的治疗选择。