上月,BridgeBio Pharma公司宣布因为1/2期临床试验临床试验数据“尚未达到变革性效果”,将不再继续推进针对先天性肾上腺皮质增生症(CAH)的AAV5基因疗法BBP-631,但将继续监测已入组的八名患者的情况。
该公司由美籍华裔经济学家罗闻全(Andrew Wen-Chuan Lo)创立,专注于罕见病和遗传性疾病的治疗方法。公司采取了一种独特的运营模式,通过建立多个子公司来推进不同的药物研发项目,每个子公司都享有半自治运营权,并共享母公司的资源。目前公司的2个产品已处于商业化阶段,3个候选产品处于3期临床试验阶段。
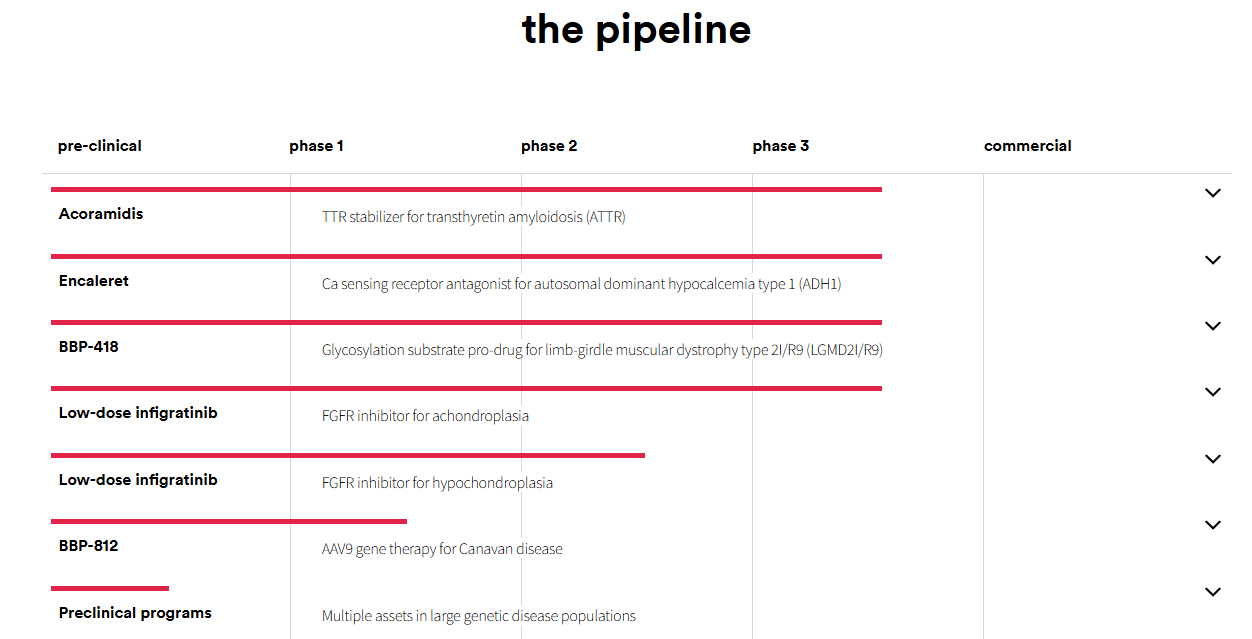
最引人注目的是,BridgeBio即将获批的药物Acoramidis,这是一种用于治疗转甲状腺素蛋白淀粉样变性心肌病(ATTR-CM)的创新小分子疗法。在3期临床试验ATTRibute-CM中,Acoramidis显示出了积极的结果,能够显著降低患者的全因死亡率和心血管相关住院的风险。
基于ATTRibute-CM试验的积极结果,BridgeBio已向FDA提交了新药申请,预计在2024年11月29日前获得审评结果。同时,他们也已向欧洲药品管理局(EMA)也接受了其上市授权申请(MAA)。
Acoramidis 3期临床成功的消息发布后,BridgeBio当日股价盘前大涨75.85%,市值暴增24亿美金,总市值超过50亿美元。
与此同时,BridgeBio Pharma在治疗Canavan(卡纳万)病方面也取得了进展。卡纳万病是一种罕见的遗传性脑白质病,目前尚无特效治疗方法(该基因疗法目前在国内招募患者参与,详情查看:卡纳万病新希望!全球基因疗法临床研究招募中国患者)。
2024年9月10日,BridgeBio Pharma宣布美国FDA已授予BBP-812再生医学高级疗法(RMAT)称号,RMAT指定是在美国FDA对研究BBP-812的CANaspire 1/2期临床试验的临床数据进行审查后授予的,BBP-812是一种在研静脉注射(IV)AAV9基因疗法,可满足卡纳万病患者尚未得到满足的医疗需求。据联邦试验数据库显示,BridgeBio的子公司Aspa Therapeutics正在一项1/2期开放标签研究中测试这种代号为BBP-812的疗法,该研究将于2026年10月结束。
BridgeBio在资本市场上表现活跃,进行了多次成功的融资。2019年,公司通过IPO融资了3.48亿美元,成为当年生物科技领域最大的IPO之一;2021年11月,BridgeBio获得了高达7.5亿美元的非稀释性债务融资;2023年9月,BridgeBio宣布了一项2.5亿美元的私募股权融资,由卡塔尔投资局(QIA)领投;今年1月,BridgeBio还获得了12.5亿美元的重大融资,这一资金主要来自Blue Owl Capital和加拿大养老金计划投资委员会(CPPIB)的子公司CPPIB Credit Investment。
BridgeBio通过这些融资活动,不仅增强了其财务状况,而且为其研发管线的推进和商业化提供了坚实的资金支持。公司的产品管线涵盖了多个治疗领域,包括遗传性心脏病、神经学、肿瘤学等,其中一些项目已经进入临床后期阶段。通过这些融资,BridgeBio能够继续推动其创新药物的研发,为患者带来更多的治疗选择。