根据国家药监局官网公示,9月以来,多款罕见病新药或新适应症的上市申请获受理,有望为纯合子型家族性高胆固醇血症、脊髓性肌萎缩症等患者带来新的治疗选择。
阿斯利康:转甲状腺素蛋白淀粉样变性
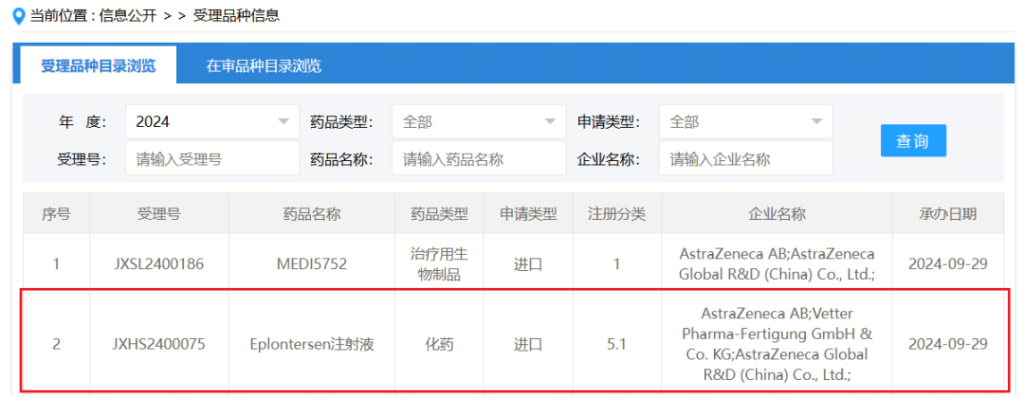
9月29日,中国国家药监局药品审评中心(CDE)官网显示,阿斯利康的反义疗法Eplontersen(IONIS-TTR-LRx,商品名:Wainua)在华申报上市。根据该药在中国的临床研究,推测其本次申报的适应症可能为:用于治疗转甲状腺素蛋白淀粉样变性心肌病(ATTR-CM)成人患者。
正大天晴:纯合子型家族性高胆固醇血症
9月27日,国家药监局药品审评中心官网公示,南京正大天晴申报的瑞舒伐他汀依折麦布片(I)上市申请获受理,适应症为用于治疗高胆固醇血症以及纯合子型家族性高胆固醇血症(HoFH)患者。截至目前,除正大天晴外,石家庄四药、福元医药、诺得药业、朗诺制药4家药企按照4类申报生产这一药物均获受理。
罗氏:脊髓性肌萎缩症
9月12日,罗氏申报的利司扑兰片上市申请获得受理,具体适应症尚未披露。利司扑兰是一款神经罕见病创新药物,为SMN2基因mRNA剪接修饰剂,用于治疗脊髓性肌萎缩症(SMA)。该药物的口服溶液剂型已在中国获批上市,用于治疗16日龄及以上的SMA患者。此次上市申请的剂型为片剂。
诺华:C3肾小球病
9月5日,诺华盐酸伊普可泮胶囊新适应症上市申请获得受理,拟纳入优先审评,适用于治疗C3肾小球病(C3G)成人患者。伊普可泮是一款特异性补体B因子口服抑制剂,已在中国获批治疗阵发性睡眠性血红蛋白尿症(PNH)成人患者。本次是伊普可泮第三次在中国申报上市。
本文来源:人民日报健康客户端