Catabasis公布的季度报表显示,依达沙龙(Edaxalonexent)治疗杜氏肌营养不良(DMD)进入提交上市申请前最后阶段,三期临床试验。
Edaxalonexent是一个口服小分子新药,正在研究治疗所有类型的DMD。
杜氏肌营养不良是由基因突变引起。患者无法产生足够营养不良蛋白。而肌营养不良蛋白为肌肉纤维提供支持, 并保护他们免受伤害。
如果没有营养不良蛋白, 肌肉纤维在每次收缩时都会受损。
依达沙龙咋工作?
健点子小编发现,依达沙龙针对的是一种名为NF-Kb的信号通路。
NF-kappa b的信号通路当DMD 患者还在儿童时就被激活。
这条信号通路的激活,造成了DMD孩子的肌肉纤维崩溃, 以及他们肌肉损伤无法得以修复。
因此,依达沙龙通过抑制NF-Kb,阻断了这条信号通路。
这样,希望是通过这个新药的作用,可以保存年幼的DMD孩子的肌肉功能,不至于继续弱化衰竭。
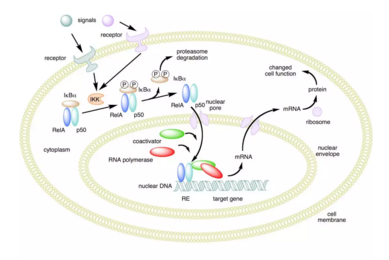
(NF-kb通路。网络照片)
三期临床细节
这个三期临床试验,PolarisDMD将是一个国际多中心试验,计划招募125名4岁至7岁的男孩DMD患者。
这些孩子至少有6个月没有接受激素治疗。
健点子ihealth查询了临床试验数据记录,表明,这个为期52周的临床试验的国家一共有7个,分别是美国,加拿大,瑞典,澳大利亚,英国,德国,爱尔兰。
此外,参加这个临床试验的患者将随机,分组,每天服用依达沙龙 (100 mg/kg 胶囊) 或安慰剂。
患者将每三个月进行一次门诊就诊, 其主要目标是在一年内改变北极星评估分数。
北极星(NorthStar)测试包括测量孩子站立时间的测试、四阶楼梯爬测试和10米步行测试。
此外,这个试验还将测试DMD男孩的肌肉力量和生长, 以及心脏和骨骼的健康。
这项研究不需要进行肌肉活检(CK)或磁共振成像 (MRI)的检测。
这个试验持续时间为52周。
一期临床试验怎样
在早先进行的一二期临床试验中,依达沙龙的表现在31名4-8岁的孩子中,评估了在基因确认诊断为 DMD 的儿童中, 依达沙龙的安全性、有效性和药代动力学 (治疗在体内的移动)。
这个MoveDMD 的试验发现,与安慰剂相比, 经依达沙龙60周的治疗,可显著缓解肌肉功能, 并大大减缓 DMD 疾病的进展。
经过一年多的治疗, 所有肌肉功能的评估都有持续的改善。
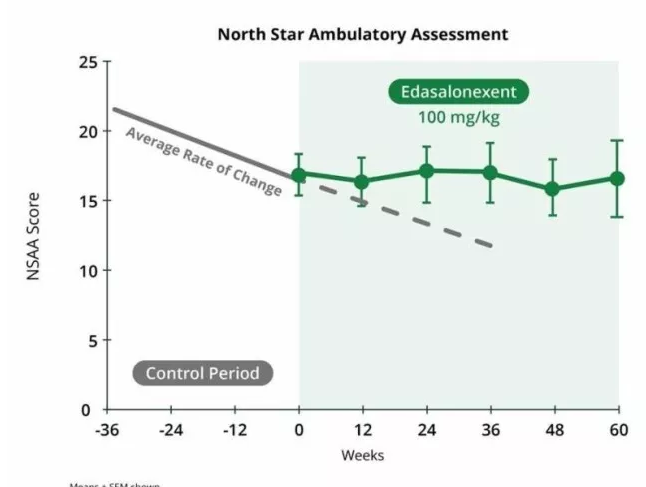
(一二期试验北极星测试结果显示,病情得以稳定)
在试验中没有观察到安全性的不良反应下, 说明,依达沙龙的耐受性良好。
美国食品药品监督管理局 (FDA) 授予了快速通道指定。欧洲联盟委员会 授予治疗 DMD 的孤儿药资格。
截至2019年3月31日的三个月中, Catabasis业务损失为630万美元, 比去年同期的760万美元损失有所减少。
下一步
试验的初步结果,预计将在2020年下半年完成后出来, Catabasis公司表示。
如果结果良好,公司计划在2021年初申请对依达沙龙进行上市注册申请。
如果获批上市,这也将是非激素,治疗所有类型的DMD的口服药的一个突破。
目前,美国食品药品监管局FDA获批治疗DMD的两个新药,一个是针对外显子51跳跃的eterplirsen,另一个是皮质激素Emflaza(地夫可特)。
此外,基因治疗所有类型突变的DMD方面,有三个基因疗法正在进行临床试验,详情请参照健点子ihealth的三朵花蕾等文章。
参考文章:
1.http://ir.catabasis.com/news-releases/news-release-details/catabasis-pharmaceuticals-reports-first-quarter-2019-financial
2. https://musculardystrophynews.com/edasalonexent/
3.https://clinicaltrials.gov/ct2/show/study/NCT03703882?term=catabasis&cond=DMD&rank=2&show_locs=Y#locn