11月5~6日,第四届亚洲庞贝病论坛在上海召开,旨在帮助国内临床医生了解庞贝病(PD)研究进展,增强罕见病筛查意识,提高诊疗水平。华中科技大学同济医学院附属同济医院罗小平教授表示,本次会议有125位来自东亚和东南亚的代表,50%参会医生或学者来自海外。来自中国大陆、香港特别行政区、台湾,阿根廷,马来西亚,新加坡,沙特阿拉伯,日本的多位儿科学、神经病学、神经生理学专家出席此次会议,并分享了PD相关研究进展和临床诊疗经验。现将会议主要内容整理以飨读者。

罗小平教授
链接
花1分钟了解庞贝病
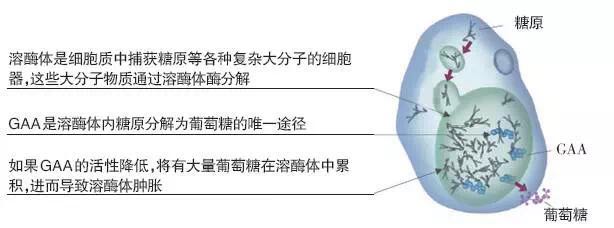
▲图1 庞贝病的病理生理学机制示意图
PD是一种罕见的常染色体隐性遗传病,由于酸性-α葡萄醣苷酶(GAA)的活性缺乏,导致糖原不能正常代谢而贮积在肌肉细胞的溶酶体中,引发不可逆的神经肌肉病变(NMD)(图1)。该病临床表型范围广泛,症状最早可能出现在1岁以前(婴儿型庞贝病,IOPD),或1岁后,如儿童、青春期及成人(晚发型庞贝病,LOPD)。进行性近端肌无力是PD最常见的症状,其次为呼吸困难、轻至中度的CK水平升高等。早期诊断和早期治疗对改善PD患者预后非常重要。
1、庞贝病发病情况之亚洲
讲者:台湾大学医学院附设医院 Paul Wuh-Liang HWU

Paul Wuh-Liang HWU教授
病理生理及表现型
胡(Paul Wuh-LiangHWU)教授在报告中指出,庞贝病的病理学机制是GAA 缺乏。GAA 缺乏导致糖原在几乎所有组织的溶酶体内贮积,尤以心肌、骨骼肌和呼吸肌最为明显。早期病变细胞含有体积较小、充满糖原的溶酶体,随疾病进展,出现糖原贮积和溶酶体扩张,发生轻度/中度肌病。溶酶体膜破裂后,糖原进入细胞质,肌肉组织出现大范围的超微结构损害,发生重度肌病。
如果患者在6个月龄内发病,病情往往较严重,出现心脏损害,称之为典型IOPD。对于典型IOPD,不给予治疗和呼吸支持,生存期一般不超过1年。研究表明,IOPD患者平均需要呼吸支持的时间在5.9个月龄时。对于LOPD患者,20~50岁都可能发病,疾病异质性很强。但是一旦出现肌肉疲弱症状,病情就会进展很快,几年之内就会出现呼吸衰竭。
亚洲患者的特殊基因型及表现型
台湾数据显示,PD发病率为1:17000,典型IOPD 发病率为1:52000。PD新生儿筛查台湾已经进行10余年,通过早期筛查治疗,IOPD患者生存期由1 年延长为10年。IOPD 患者存在基因变异,纯合子变异率在日本为3.9% ,在台湾为3.69%,这种变异是一种假基因缺失,可以降低GAA的活性。目前中国已有一些基础和临床研究。27例中国LOPD患者(平均发病年龄22岁)中,GAA基因发生26种变异,其中10项为新发现。18 例中国IOPD患者(平均发病年龄3.6个月,平均诊断年龄6.3个月)的基因型也有相关分析报告。
2、庞贝病发病情况之中国
讲者:北京协和医院 邱正庆

邱正庆教授
中国数据
2005~2016年中国大陆共发表PD相关文章53篇,确诊患者199例。其中,北京和上海确诊的患者分别占44%、39%,广州占8%,其他地区占8%,提示,患者主要在中国大陆的一线城市得到确诊。确诊科室主要是儿科和神经科。这些文献中,初始诊断方法主要通过白细胞或干血纸片法(DBS)测定GAA活性。
数据还显示,IOPD平均确诊时间为发病后3.6个月,而LOPD患者确诊时间则长达5年。17.7%IOPD、22% LOPD患者有家族史,磷酸肌酸激酶(CK)水平波动范围很大。对患者进行肌肉活检,显示,患者肌纤维中有充满糖原的空泡,空泡密度存在个体差异。PD患者GAA活性显著低于正常个体,中国LOPD患者的DBS GAA活性的中位数仅为2.7 pmol/punch/h,而这一数据在正常个体为36.37 pmol/punch/h,在携带者为24.77 pmol/punch/h。此外,山东大学医学院附属齐鲁医院的8 例LOPD患者中,有3例伴有脑血管疾病。
中国大陆与其他国家或地区数据对比
国外研究显示,心脏问题是IOPD患者首次就诊的主要原因,但对LOPD患者而言,肌肉疲弱是首次就诊的主要原因,中国患者与此相似。基因突变方面,c.1935C>A(p.Asp645Glu)是IOPD较常见的突变基因(25%),c.2238G > C(p.W746C)是LOPD较常见的突变基因(27%),与中国台湾一致。此外,c.-32-13 T > G是高加索人最常见的突变基因,但仅在中国一位患者中发现了杂合子突变。另外在韩国、葡萄牙、日本、亚裔美国人中的一些较常见突变基因也并未在中国患者中检测到。
3、婴儿型庞贝病
典型病例
讲者:新加坡妇女儿童医院 Ee Shien TAN

Ee Shien TAN副教授
谭(Ee Shien TAN)副教授介绍,一名女婴,其母亲妊娠时检查无异常,顺产,4个月大时出现发育迟缓,表现为体重增长缓慢、舌头肥大,就诊于儿科。7个月时未出现好转,考虑甲减,转诊治内分泌科,但治疗无效,患者出现支气管炎(咳嗽、发烧),颈部肌肉无法支撑头部,转诊至神经科。给予胸透检查发现心脏肥大,心脏科医生会诊,给予进一步2D超声心动图检查发现,患者双心室肥大、心肌舒缩无力。营养科医生发现其肌张力减退、反应迟缓、甲状腺功能正常,考虑椎体肌肉萎缩,但活检后未找到病因。后又进行一系列检查,发现患者脂肪代谢不正常,GAA缺乏,综合以上情况诊断为IOPD。该患者从症状出现到诊断为IOPD历时4个月,经过5个专家会诊。给予酶替代疗法(ERT)后,患者可以坐起,在帮助下可以站立,但因为诊断和开始治疗较晚,无法走路,不能达到最佳状态。
诊断方法介绍
讲者:台湾大学医学院附设医院儿科 Paul Wuh-Liang HWU
怀疑IOPD
对婴儿除外的患者,肌肉活检和CK水平升高、呼吸衰竭时,即使症状轻微,也应考虑PD并进一步检查GAA酶活性。对婴儿而言,当其出现“懒散”、心肌症状时,应警惕IOPD。一些地区目前已开展IOPD新生儿筛查,可明显增加诊断率。
进行排除性检查
CK水平升高提示肌肉损伤。事实上,在PD患者中,CK水平上升并不明显。很多疾病会造成CK水平忽高忽低,如轻微外伤。临床中可对CK水平进行追踪,如果CK水平升高,但没有突破上限,并不能说明问题。但应通过肌肉活检和干血斑(DBS)GAA活性检查进一步排除PD早发导致的症状不明显的情况。
进行确诊性检查
确诊PD的血液学检查方法有检测CK 水平、DBSGAA和全血GAA活性试验、GAA基因测序。肌肉活检可以观察特殊组织染色病理切片以及进行肌肉GAA活性检查。值得一提的是,在检查全血GAA活性时可能会遇到一些问题。血液中不仅有GAA,还有麦芽糖酶糖化酶(MGA)和中性α-葡萄糖苷酶(NGA),成功分离这三种酶可提高检测准确性。HWU教授对每种检查方法及可能遇到的问题、局限性进行了详细的解释和说明,并表示,PD疾病诊断充满挑战,应联合使用多种诊断工具。
早期诊断和新生儿筛查的重要性
讲者:台湾大学 Yin-Hsiu CHEN

Yin-Hsiu CHEN教授
陈(Yin-Hsiu CHEN)教授指出,早诊断早治疗IOPD非常重要。如果不及时治疗,当溶酶体过于膨胀使糖原泄露进细胞质时,会对肌细胞造成严重损害,且对重组人酸性α-葡糖苷酶(rhGAA)的应答降低。患者出现症状后中位确诊时间为4个月,但IOPD患者的父母能够在2个月时就观察到婴儿的变化,因此,建议提高公众对这一疾病的知晓率。临床医生在未确诊时,会通过观察来明确诊断,这段“观察时间”会对IOPD患者预后带来显著影响。相比依赖公众认识和临床诊断效率,进行新生儿筛查是更有效的方法。通过新生儿筛查诊断为IOPD、交叉反应免疫物质(CRIM)阳性的患者,在出生后2周或2个月时开始给予rhGAA治疗,患者生存率显著增加,大部分患者后期不需要呼吸机支持,且能够完成基本的运动。
IOPD患者的治疗与管理
讲者:台湾大学 Yin-Hsiu CHEN
IOPD患者心脏肥大通过rhGAA治疗4个月后有望恢复正常。虽然心脏损害可逆,但会有心律不齐情况持续,应密切观察,适当干预。患者的肌力通过6分钟步行测试(6MWT)进行评估、帮助做一些拉伸训练,尽量保持运动能力。此外,治疗中会发现有些患者CK水平依然较高,要根据情况调整用药剂量。呼吸方面,建议对患者呼吸功能进行观察。给予流感疫苗,避免进一步加重其呼吸系统负担。此外,糖原还存在于神经细胞中,可能会影响听力,必要时戴助听器。因此,IOPD患者的治疗和管理需要神经科、营养科、儿科、耳鼻喉科、心理科等多学科的合作。
4、晚发型庞贝病
神经内科医生在罕见神经肌肉疾病中的角色
讲者:沙特阿拉伯费萨尔国王专科医院研究中心 Edward James CUPLER

Edward James CUPLER教授
向患者传达检查的重要性
在沙特阿拉伯,主要由政府承担医疗费用,但是患者还是因为各种各样的检查而感到困惑。因此,医生应向患者传达检查的重要性,只有明确诊断,才可以有更好的治疗,并让患者认识到接受“管理”直到治愈的意义。
神经科医生的诊断思路
作为神经科医生,对LOPD患者进行管理和指导时,首先对患者进行临床检查。其次,要了解指南中的建议和推荐。2009年LOPD指南中,对LOPD患者的临床表型颇有争议。患者可能出现肢体乏力,但并不能给医生太多提示。肱四头肌、腹部肌群、中轴肌、背阔肌等所涉及的疾病较少,医生往往也不会意识到检查这些肌肉。神经内科医生应该在这些方面进一步改进。
CK水平可作为参考指标。CK水平波动范围非常大,可达正常值的15倍,CK 升高患者中约有2%是LOPD。在进一步检查中,患者的肺活量(FVC)是重要指标,如果仰卧位FVC 下降超过10%,可怀疑LOPD。很多LOPD 患者伴有膈肌无力。肌电图(EMG)可见肌细胞膜易激、肌强直电位等。肌肉活检显示肌肉组织被糖原填充。DBS可以帮助进一步诊断。
卡布(Edward JamesCUPLER)教授还介绍了新一代测序(NGS)基因芯片技术,如果用于PD检查将会对诊断非常有帮助。
识别LOPD患者面临的挑战
讲者:山东大学医学院附属齐鲁医院 焉传祝

焉传祝教授
肌肉疲弱患者应排查LOPD
对LOPD 患者,医生面临的较大挑战就是尽早明确诊断,数据显示LOPD从发病到诊断可能需要8~12年之久。LOPD可以累积肩带肌、中轴肌、腹肌、臀大肌等多处肌肉组织,1/3患者会出现近端肌肉的疲弱,2/3患者伴有远端和中轴肌肉的疲弱,因此,在任何不明确的肌肉疾病中都应该将LOPD考虑在内。
对肢带型肌无力(LGMW)患者,进一步检查可能会发现其出现呼吸不畅等症状。但是这些症状依然可以体现在其他疾病中,如侧索硬化性疾病、多发性肌炎等。然而,出现这些症状时,应排查LOPD。
年轻卒中患者应排查LOPD
临床中两例LOPD患者出现脑血管收缩不良和脑动脉栓塞、小动脉缩窄等症状。另一例患者出现了基底动脉瘤。因此,对于年轻卒中患者中的鉴别诊断中应该排查LOPD。
GAA 活性检测是诊断LOPD的金标准
焉传祝教授详细介绍了LOPD的一般临床诊疗思路(图2)。他指出,为了进一步明确LOPD诊断,需要进行肌肉活检、GAA活性和基因检测。其中,肌肉活检阴性并不能排除LOPD,GAA 活性检测是诊断PD的金标准,DBS是诊断GAA活性的主要方法,具有微创、简单、样本稳定等优点,诊断敏感性为100%,但存在5.2%的假阳性率。NGS基因芯片分析技术具有较高敏感性(100%)和特异性(98%),可作为确诊LOPD 患者GAA基因突变的首选。
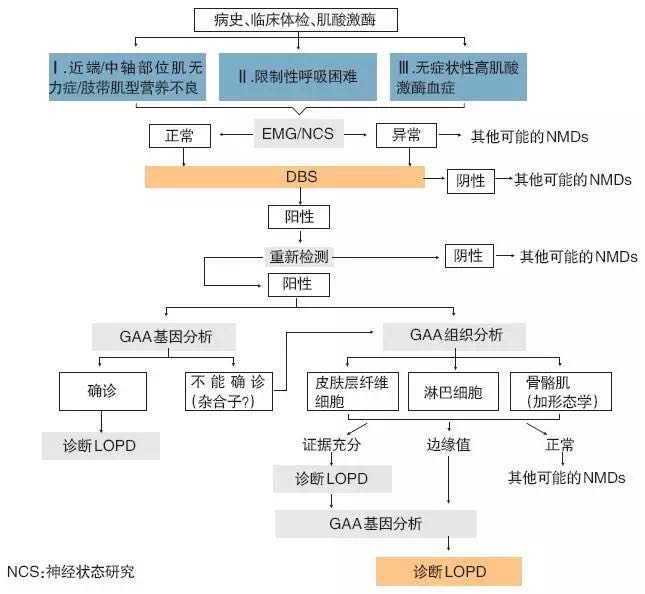
▲图2 庞贝病临床诊疗思路
肌肉诊断工具的角色
讲者:日本国立神经肌肉学研究中心 Ichizo NISHINO

Ichizo NISHINO教授
肌肉诊断工具的特点
尼希诺(IchizoNISHINO)教授指出,肌肉疾病诊断工具有很多种,包括病原学检测、生物化学检测、基因检测、影像学检查、电镜生理学检查等。通过病原学检查可以将肌肉疾病分为肌肉疲弱、先天性肌病、炎症性肌病、其他疾病。肌肉活检是诊断肌肉相关疾病的主要手段。对LOPD患者,提取特殊肌组织纤维,显微镜下发现组织中有大量空泡,但有些LOPD患者肌肉活检并不典型,与IOPD情况有所不同,给确诊带来困难。
如果医生怀疑患者为LOPD,应该进行DBS 试验,基本能够确诊。基因分析是为了做确诊性诊断,目前我们也有NGS技术,但是比较昂贵。因为日本LOPD流行率非常低,所以诊断还是以DBS为主。
肌肉影像学检查的意义
在肌肉成像方面,主要采用肌肉CT、核磁共振(MRI)、超声三种方法,超声很普遍,诊断特异性不高。MRI检查有些地区很难实现,而且要全麻,给患者带来更高风险。所以,CT全身扫描可以观察患者的肌肉萎缩情况,是经济有效的方法。通过影像学诊断可以发现,LOPD患者远端肌肉保存较好,但近端肌肉、中轴肌肉、膈肌、舌肌会出现变化。
rhGAA药物的问世,为PD患者带来治疗希望,也对临床医生的诊疗水平提出挑战。目前,中国临床医生对PD的了解还不够多,存在误诊漏诊的现象。罗小平教授指出,注射用阿糖苷酶(美儿赞,活性成分为rhGAA)作为PD特效治疗药物,将于2017年在中国大陆上市,对PD这一疾病,应多学科跨界合作,以实现早期诊断,早期治疗,早期管理,改善患者预后。(飞燕)