重症肌无力(MG)是一种典型的抗体介导的自身免疫性疾病,其致病核心在于表达B细胞成熟抗原(BCMA)的浆细胞分泌致病性自身抗体,导致神经肌肉接头处的突触后膜受损。尽管近年来补体抑制剂和FcRn拮抗剂的出现为患者提供了更多选择,但仍有相当一部分患者处于难治状态或面临长期免疫抑制带来的感染风险和生活质量下降。而在血液瘤种显示出可靠治疗潜力的CAR-T细胞疗法因其高度个性化、强烈免疫激活、伴随显著毒性等特质,始终与慢性自身免疫疾病之间始终存在难以跨越的鸿沟。
在此背景下,2026年1月7日,美国休斯顿卫理公会医院、宾夕法尼亚大学、堪萨斯大学医学中心及多家科研机构团队联合在期刊Nature Medicine发表论文“BCMA-directed mRNA CAR T cell therapy for myasthenia gravis: a randomized, double-blind, placebo-controlled phase 2b trial”,披露了全球首个针对重症肌无力的BCMA定向mRNA CAR-T细胞疗法——Descartes-08的随机、双盲、安慰剂对照2b期临床试验(MG-001 part 3)数据。这一新型疗法无需清淋预处理、采用非整合mRNA技术,不仅在疗效上展现出惊人的持久性,更凭借其独特的非整合性特征,为自身免疫病的细胞治疗开辟了安全且高效的新路径。

治疗机制的范式转移
重症肌无力的核心病理在于B细胞成熟抗原(BCMA)表达的浆细胞分泌了攻击自身组织的抗体,尤其是针对乙酰胆碱受体(AChR)的抗体。基于此,Descartes-08的设计理念非常明确:通过自体T细胞表达靶向BCMA的嵌合抗体受体,精准定点清除这些“抗体工厂”。
与传统用于血液肿瘤的CAR-T疗法不同,Descartes-08采用了mRNA转染技术而非病毒载体。这种选择具有深远的临床意义:mRNA产生的CAR蛋白表达是瞬时的,这避免了T细胞在体内的无限制增殖,从而大幅降低了细胞因子风暴(CRS)和神经毒性(ICANS)的风险。更重要的是,该疗法无需进行化疗预处理(淋巴耗竭),患者可以在门诊环境下完成每周一次、共六次的静脉输注,极大地提升了治疗的可及性与患者的耐受度。
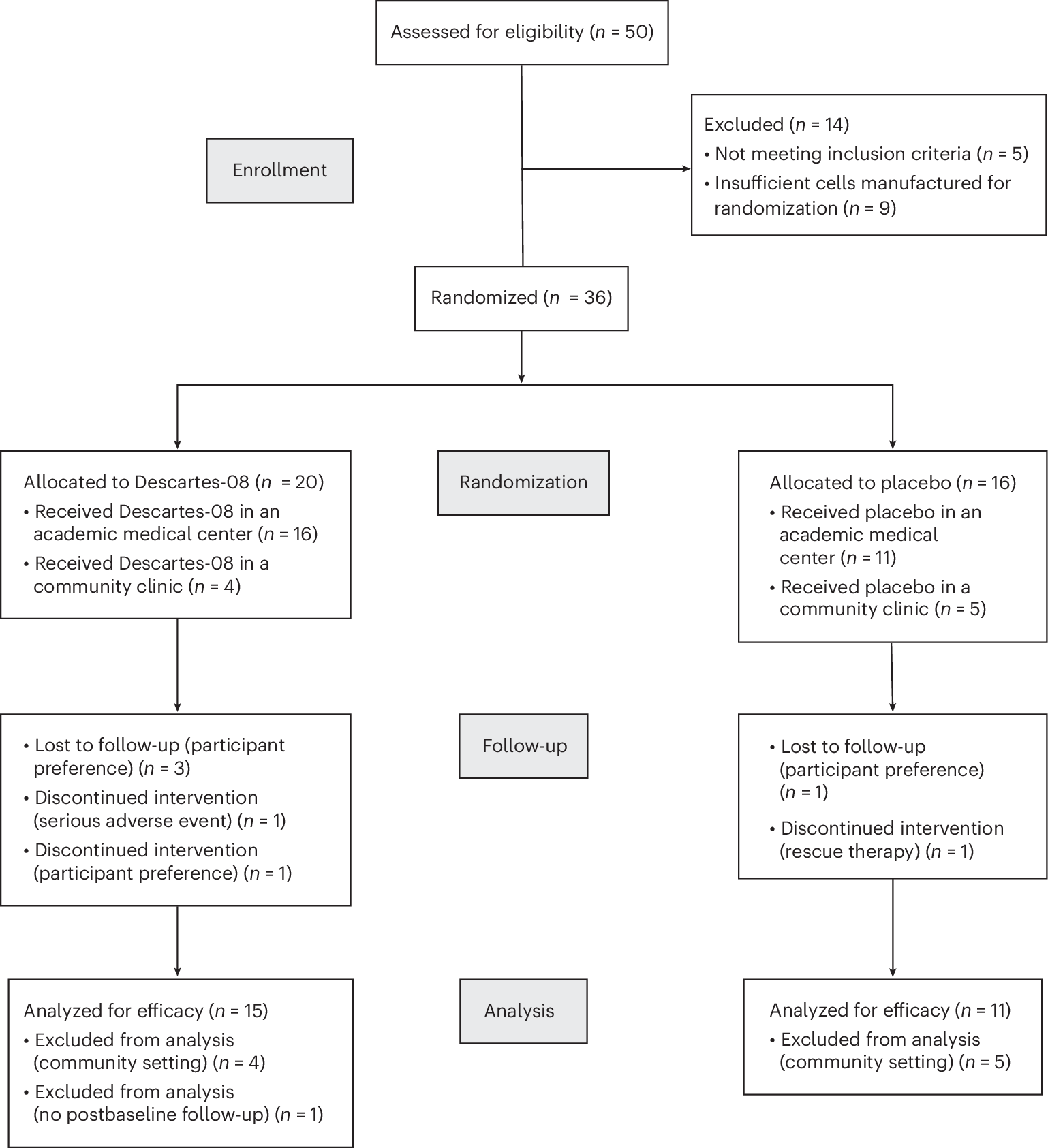 图:MG-001 part 3的试验设计
图:MG-001 part 3的试验设计
核心临床数据:
一次疗程,带来至少一年的临床获益
表:第3个月MGC、MG-ADL和QMG评分较基线的平均变化
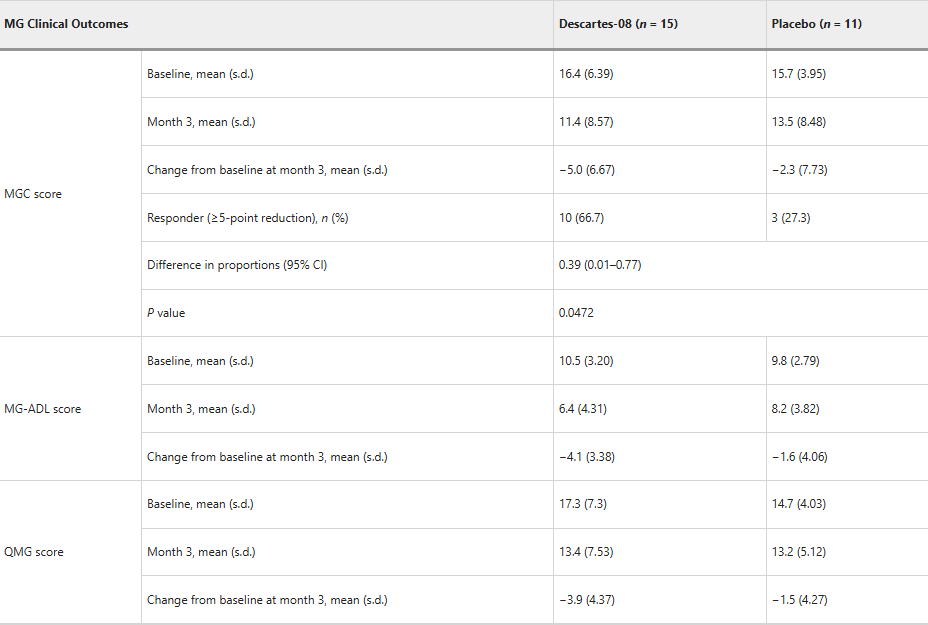
更具说服力的是疗效的持续性。接受 Descartes-08 治疗的患者,其MGC评分、生活质量量表(MG-ADL)和定量评分(QMG)在随访过程中持续改善。在第4个月时,三个数据分别较基线平均下降-7.1、-5.5和-4.8。而即便在停止输注后的数月,患者的症状仍在持续改善。到第12个月时,83.0%的患者仍维持着具有临床意义的缓解。此外,33.0%的患者在第6个月时达到了“最小症状表达”(MSE,即MG-ADL评分≤1)的状态,并且这种极佳的临床状态一直持续到了第12个月。对于那些此前未接受过生物制剂治疗的患者,MSE的达成率更是高达55.6%。这提示 mRNA CAR-T 可能在疾病早期干预中具有更大的重塑潜力。
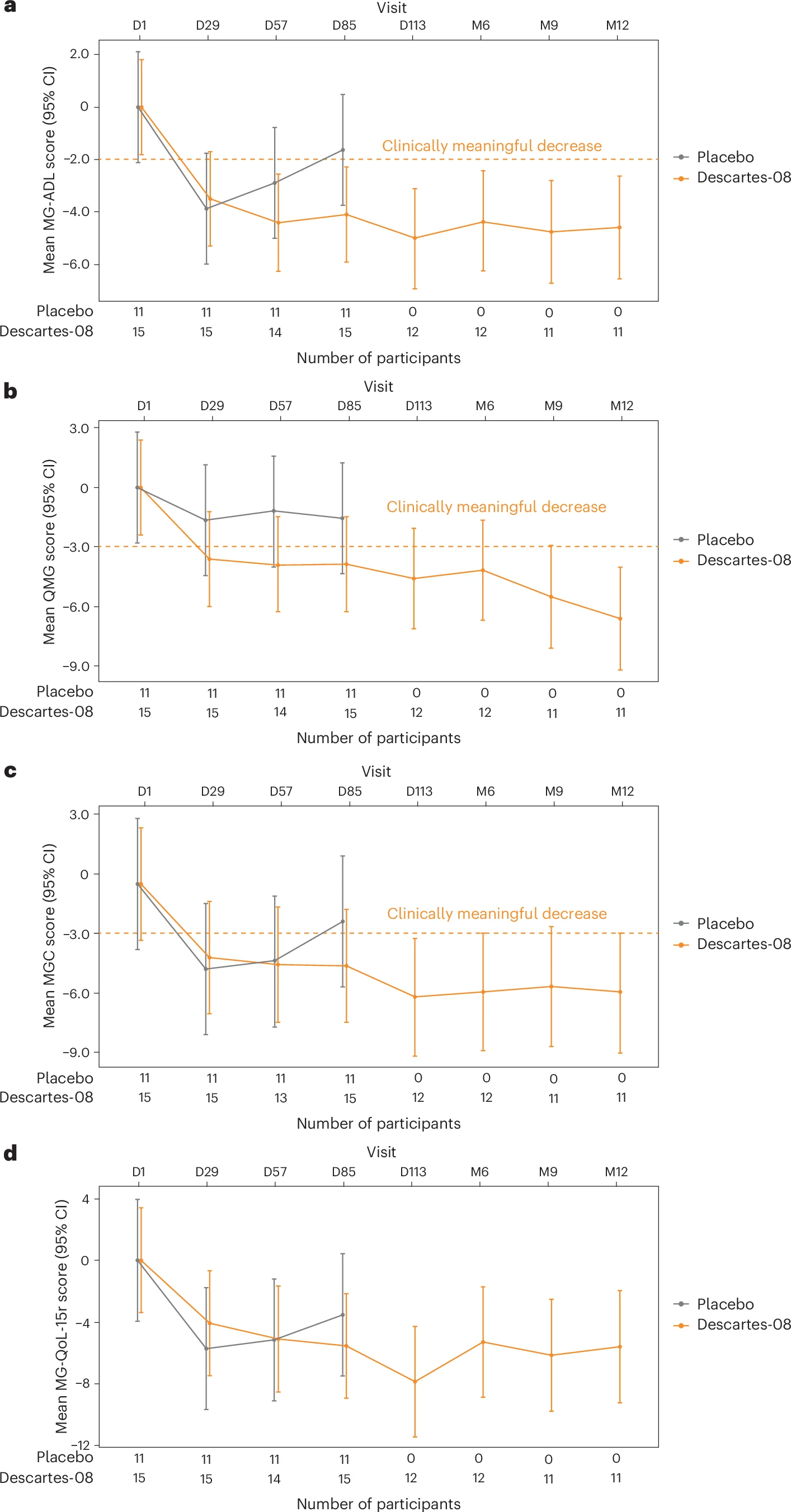
图:研究期间疾病严重程度评分相对基线的变化情况
安全性评估:
不像 CAR-T 的 CAR-T
在安全性方面,Descartes-08展现出了与传统CAR-T截然不同的优异属性。
试验中没有发生4级或5级的不良事件,也没有观察到典型 CAR-T 治疗中令人担忧的 CRS 或 ICANS。最常见的副作用是输注相关反应(IRR),主要表现为输注后8小时内出现的短暂头痛、恶心、发热和寒战,通常在24小时内无需特殊处理(如使用托珠单抗或类固醇)即可自行缓解。在整个随访期间,研究团队观察到患者体内的B细胞水平并没有发生明显损耗,也没有出现低丙种球蛋白血症。这一发现对于慢性病患者的长期安全性尤为关键,因为它意味着Descartes-08在清除致病浆细胞的同时,保留了患者基础的免疫防御能力,并未导致广谱的免疫抑制。
重塑免疫微环境
该研究还通过深度免疫监测发现,虽然Descartes-08并未引起循环中广谱炎性细胞因子的剧烈波动,但却特异性地降低了与自身免疫密切相关的细胞因子水平,如IL-6、IL-24和CCL19等。
这种免疫状态的微调反映在了患者的用药需求上。在随访12个月后,Descartes-08组患者的口服泼尼松等效剂量中位数从基线的20 mg大幅降至9 mg,降幅达55.0%。值得注意的是,在整个研究过程中,没有任何一名接受Descartes-08治疗的患者需要因为症状加重而进行静脉注射免疫球蛋白(IVIg)或血浆置换等急救治疗。
这表明mRNA CAR-T疗法不仅能改善症状,更有潜力作为一种“疾病修饰疗法”,改变重症肌无力的长期管理模式。
总结
尽管本研究受限于2b期试验的样本量,部分次要终点的比较仍具有描述性性质,但其提供的初步证据已足够强力。目前,一项针对AChR抗体阳性患者的大规模3期确认性临床试验(AURORA)已经启动,将进一步验证其在更大规模人群中的疗效。同时,mRNA CAR-T的技术框架也正在被探索用于青少年皮肌炎等其他自身免疫性疾病。
总而言之,Descartes-08的成功证明了mRNA技术在细胞治疗领域的巨大潜力。通过精准打击致病靶标,同时规避病毒载体带来的长期安全隐患和昂贵的住院成本,这种疗法为那些深受慢性自身免疫病困扰的患者提供了一种全新的、极具吸引力的“一站式”解决方案。随着后续研究的深入,mRNA CAR-T或许将彻底重塑我们治疗重症肌无力乃至更多复杂自免疾病的医学范式。
参考资料
Vu, T., Durmus, H., Rivner, M. et al. BCMA-directed mRNA CAR T cell therapy for myasthenia gravis: a randomized, double-blind, placebo-controlled phase 2b trial. Nat Med (2026). https://doi.org/10.1038/s41591-025-04171-y