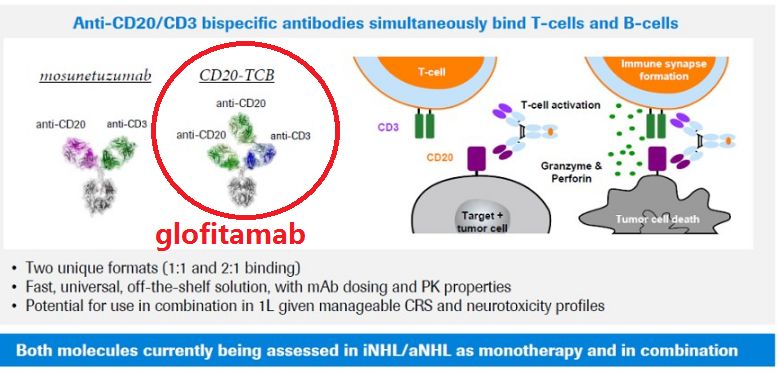
glofitamab(前称CD20-TCB)结构特征
根据美国食品和药物管理局(FDA)孤儿药数据库最新数据,罗氏(Roche)2款抗癌药已获得孤儿药资格(ODD):(1)glofitamab(前称CD20-TCB)用于治疗套细胞淋巴瘤(MCL);(2)pralsetinib用于治疗转移性RET融合阳性实体瘤。
glofitamab是一款新型CD20xCD3 T细胞结合双特异性抗体,目前正被开发用于治疗多种类型的淋巴瘤。glofitamab可同时结合恶性B细胞表面的CD20和T细胞表面的CD3,使T细胞靠近肿瘤细胞并消除肿瘤细胞。glofitamab具有一种“2:1”的新颖结构模式,含有2个靶向CD20的Fab区,一个靶向结合CD3的Fab区。
glofitamab具有的双重靶向作用,可激活和重新定向患者现有的内源性T细胞,结合并通过向目标B细胞内释放毒性蛋白来消除这些恶性B细胞,为淋巴瘤治疗提供了一种创新的方法。之前公布的数据显示,glofitamab已在多种类型的非霍奇金淋巴瘤(NHL)中显示出了良好的治疗反应。
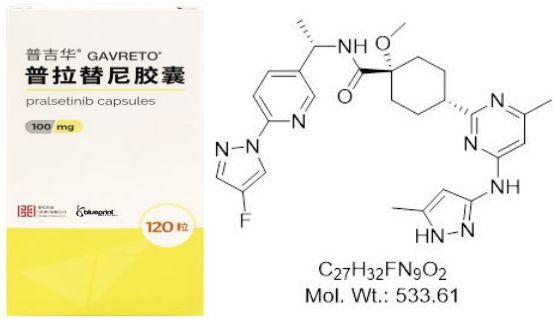
Gavreto(中文商品名:普吉华®,通用名:pralsetinib,普拉替尼)
pralsetinib(普拉替尼)是一款精准肿瘤学药物,该药是一种口服、每日一次、强效高选择性RET抑制剂,旨在抑制导致多种癌症的RET改变(融合和突变,包括预测的耐药突变)。pralsetinib已显示出治疗多种类型实体瘤的疗效,反映了不限癌种(tumour-agnostic)的潜力。
pralsetinib(普拉替尼)是由Blueprint Medicines的研究团队依据其专有化合物文库所设计的。在临床前研究中,pralsetinib针对最常见RET基因融合、激活突变和耐药突变始终表现出次纳摩尔水平的效价。此外,pralsetinib对RET的选择性与已批准的多激酶抑制剂相比有显著提高,其中,对RET有效性与VEGFR2相比有超过90倍的提高。通过抑制原发和继发突变,pralsetinib有望克服和预防临床耐药性的发生。这种治疗方法预期可以在携带不同RET变异的患者中实现持久的临床缓解,且具有良好的安全性。
2020年7月,罗氏与Blueprint Medicines签订了一项17亿美元的许可及合作协议,获得了Gavreto在美国以外地区(不包括大中华区)的独家权利、美国市场的联合商业化权利。根据之前与Blueprint签订的协议,基石药业拥有Gavreto在大中华区的独家授权。
在美国,pralsetinib(商品名:Gavreto)已获批3项适应症:(1)用于治疗经FDA批准的检测方法检测证实为转移性RET融合阳性NSCLC成人患者;(2)用于治疗需要系统性治疗的晚期或转移性RET突变甲状腺髓样癌(MTC)成人和12岁及以上儿童患者;(3)用于治疗需要系统性治疗且放射性碘难治(如适用)的晚期或转移性RET融合阳性甲状腺癌成人和12岁及以上儿童患者。
在中国,Gavreto(普吉华,普拉替尼)已获得国家药监局(NMPA)批准,用于治疗既往接受过含铂化疗的转染重排(RET)基因融合阳性的局部晚期或转移性NSCLC成人患者。Gavreto(普吉华,普拉替尼)针对需要系统性治疗的晚期或转移性RET突变MTC,以及需要系统性治疗且放射性碘难治(如放射性碘适用)的晚期或转移性RET融合阳性甲状腺癌的新适应证申请也已经于2021年4月获得NMPA受理并被纳入优先审评。
原文出处:Orphan Drug Designations and Approvals