Mirum Pharma是一家致力于开发创新疗法治疗罕见肝脏疾病的生物制药公司。近日,该公司宣布,美国食品和药物管理局(FDA)已批准Livmarli(maralixibat)口服液,该药每日口服一次,用于治疗年龄≥1岁的Alagille综合征(ALGS)患者的胆汁淤积性瘙痒。ALGS是一种罕见的遗传性肝脏疾病,在美国影响2000-2500名儿童。
ALGS由胆管异常引起,可导致进行性肝病。胆管异常或狭窄会导致胆汁淤积,胆汁酸在肝脏中积聚,从而导致炎症和肝损伤,并阻止肝脏正常工作。ALGS的胆汁淤积与瘙痒相关。瘙痒是与ALGS相关的最常见和最严重的症状之一,也是ALGS患者进行肝移植的最常见指征之一。
值得一提的是,Livmarli是第一个也是唯一一个被批准用于治疗ALGS胆汁淤积性瘙痒的药物,将为ALGS治疗模式带来一个有意义的转变。Livmarli通过优先审查程序获得批准。此前,FDA已授予Livmarli治疗ALGS的罕见儿科疾病资格(RPDD)和突破性药物资格(BTD)。
在批准Livmarli的同时,FDA还颁发给Mirum公司一张罕见儿科疾病优先审查凭证(PRV),以奖励该公司在罕见病新药研发方面做出的突出贡献。这张PRV可以兑换以获得任何后续新药申请的优先审查,并且可以出售或转让。
Livmarli口服液的活性药物成分为maralixibat,这是一种口服给药、具有最小化吸收的回肠胆汁酸转运体(IBAT)抑制剂。ALGS是一种罕见的肝脏疾病,尚无公认的治疗方法,因此存在着重大而紧迫的未满足医疗需求。Livmarli的批准上市,将为这一毁灭性的疾病带来有史以来第一个药物治疗选择,将提供一个有意义的治疗方案,最终将减少肝移植的需求。
FDA批准Livmarli,基于关键ICONIC研究以及来自支持性研究的5年数据,这些数据共同组成了Livmarli治疗86例ALGS患者的强有力证据体。来自ICONIC研究的数据显示:接受Livmarli治疗后,患者瘙痒在统计学上显著减少(p<0.0001)、其他胆汁淤积性肝病标志物得到改善。
Mirum总裁兼首席执行官Chris Peetz表示:“今天对于ALGS社区来说是一个伟大的日子,FDA批准了一个急需的新治疗方案,以解决该疾病最令人虚弱的影响之一。我们感谢推进这项研究并参与Livmarli临床研究的患者、家属和医疗专业人员。今天也是Mirum里程碑式的一天,因为我们在开发治疗罕见肝病的潜在改变生命的药物方面迈出了一步。”
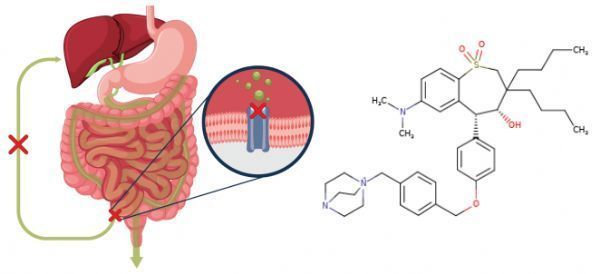
maralixibat是一种新型的、最小化吸收的、口服回肠胆汁酸转运体(IBAT)抑制剂,正在对几种罕见的胆汁淤积性肝病进行评估。maralixibat可抑制顶端钠依赖性胆汁酸转运体(ASBT),导致更多胆汁酸在粪便中排出,导致系统性胆汁酸水平降低,从而潜在地减少胆汁酸介导的肝损伤及相关影响和并发症。
Alagille综合征(ALGS)是一种罕见的遗传性疾病,由胆管异常(狭窄、畸形、数量减少)引起,导致肝脏内胆汁积聚,最终发展为肝脏疾病。据估计,ALGS的发病率为每30000人中就有一例。在ALGS患者中,多个器官系统可能会受到突变的影响,包括肝脏、心脏、肾脏和中枢神经系统。
胆汁酸的积累妨碍了肝脏正常工作,以排除血液中的废物,根据最近的报道,60%-75%的ALGS患者在成年前接受了肝移植。ALGS肝损伤引起的体征和症状可能包括黄疸(皮肤变黄)、黄瘤(使皮肤下胆固醇沉积变形)和瘙痒。ALGS患者所经历的瘙痒是所有慢性肝病中最严重的,并且在大多数受影响的儿童中在3岁时出现。
除了ALGS之外,maralixibat也正处于后期临床开发,用于治疗其他罕见胆汁淤积性肝病,包括进行性家族性肝内胆汁淤积症(PFIC)和胆道闭锁。之前,FDA也授予了maralixibat治疗这2种疾病的突破性疗法认定(BTD)和孤儿药资格(ODD)。
原文出处:U.S. FDA Approves LIVMARLI (maralixibat) as the First and Only Approved Medication for the Treatment of Cholestatic Pruritus in Patients with Alagille Syndrome One Year of Age and Older
版权声明:本网站所有注明“来源:罕见病信息网”的文字、图片和音视频资料,版权均属于罕见病信息网网站所有。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。