克拉伯病 (Krabbe disease, KD) 又称球形细胞脑白质营养不良,是一种由半乳糖脑苷酯酶 (galac‐tocerebrosidase, GALC) 缺乏导致的罕见常染色体隐性遗传溶酶体贮积病。据统计,克拉伯病的发病率约为1/10万,临床上以早婴型多见 (占85%~95%),主要表现为哭闹无法安抚、易激惹、肌张力增高、严重的认知功能和运动技能倒退,患儿极少存活超过2年,亟需开发新型的创新疗法。
近日,来自韩国首尔国立大学的研究团队利用双AAV9载体递送腺嘌呤碱基编辑器ABE8e,在小鼠模型上首次实现了对克拉伯病致病基因GALC的体内单碱基精准修复,显著恢复酶活、减少神经毒性、保护髓鞘、延长动物生存期,为这类无药可医的致命性溶酶体贮积症开辟 “一次治疗、长期治愈” 的全新路径。
▲ 来源: istock
关键突破:极低编辑效率即可产生强效治疗获益
克拉伯病 (Krabbe disease, KD) 又称球形细胞脑白质营养不良,是一种罕见的常染色体隐性遗传性溶酶体贮积病,其病因为半乳糖脑苷脂酶 (galac‐tocerebrosidase, GALC) 的功能不足,导致半乳糖基鞘氨醇等有毒代谢产物在中枢和周围神经系统中积聚,引起神经脱髓鞘病变,引发严重的神经功能障碍。婴儿型病例病情迅速进展,导致早期死亡,因此早期诊断和干预至关重要。而成人型呈现异质性,易漏诊和误诊,给临床管理带来极大挑战。

▲ 论文截图
2026年4月23日,来自韩国首尔国立大学的研究团队在Genome Medicine上发表题为In vivo adenine base editing of mutant Galc gene ameliorates Krabbe disease progression (体内腺嘌呤碱基编辑突变Galc基因可改善克拉伯病进展) 的研究论文。研究团队针对GALC基因355位密码子G→A 点突变产生的提前终止密码子,利用双AAV9载体递送不造成DNA双链断裂、更安全高效腺嘌呤碱基编辑器ABE8e,在Twitcher (Galc twi/twi ) 小鼠模型中首次实现了对克拉伯病致病基因GALC的体内单碱基精准修复,显著恢复酶活、减少神经毒性、保护髓鞘、延长动物生存期,为这类无药可医的致命性溶酶体贮积症开辟 “一次治疗、长期治愈” 的全新路径。
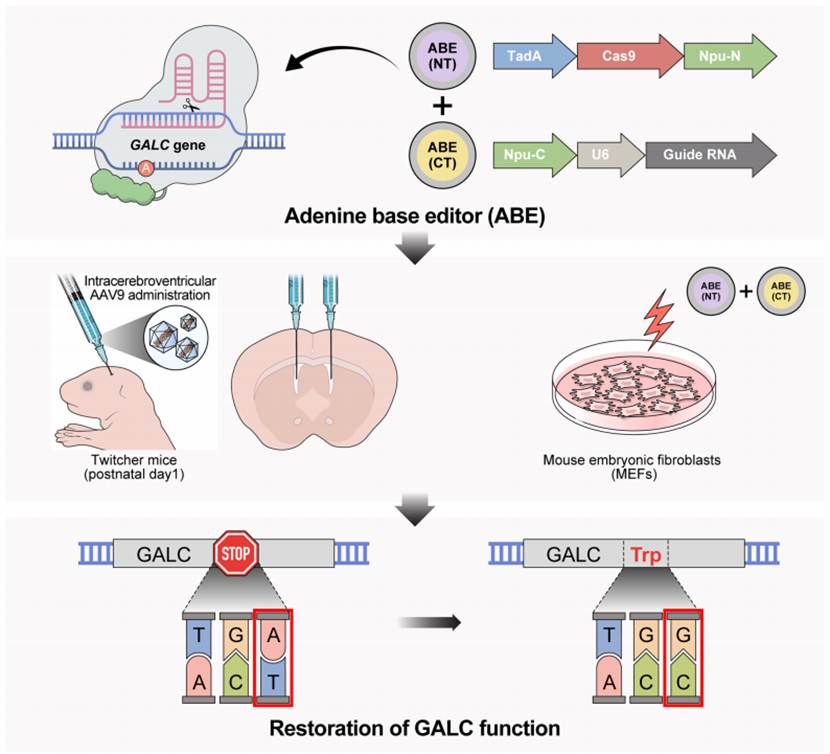
▲ 机理模式图
研究发现,即使基因组水平校正效率仅约0.5%,mRNA水平校正率约5%,即足以恢复GALC蛋白功能并阻断疾病进程。GALC酶活性恢复至野生型对照组的约5%,达到溶酶体贮积病中经临床前与临床证据验证的有效治疗阈值 (通常为3%–5%)。于此同时,髓鞘结构完整性显著改善,胼胝体G-ratio提升59%,提示脱髓鞘减轻及髓鞘再生增强,中位生存期延长20%–30%,且未检测到脱靶碱基编辑、免疫原性反应或神经炎症等安全性风险。
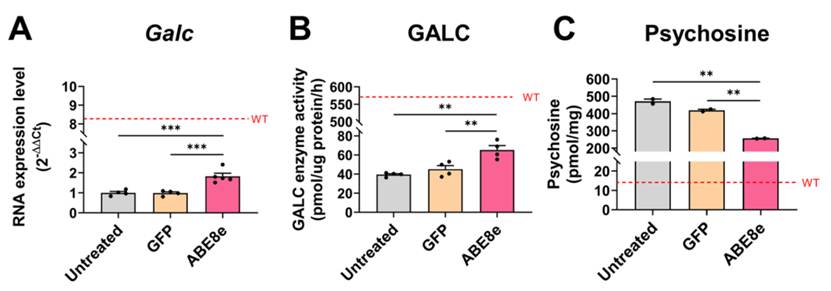
▲ 临床前数据
为系统评估潜在的脱靶风险,研究团队依据严格设定的脱靶预测参数(允许最多3个碱基错配及1个DNA/RNA凸起),共鉴定出12个高置信度脱靶候选位点。在针对额叶皮质与胼胝体两个关键脑区,分别检测各脱靶位点中位于ABE8e活性窗口内的靶向腺嘌呤残基。结果显示,在未处理对照组、GFP阴性对照组及ABE8e治疗组中,所有12个预测脱靶位点的编辑率均低于0.3%,未观察到具有生物学意义的脱靶碱基编辑事件。
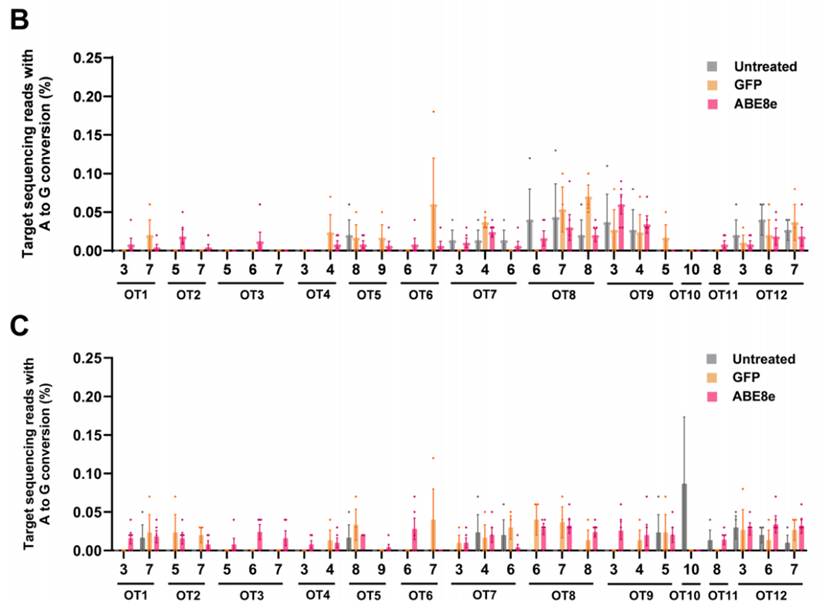
▲ 临床前数据
本研究首次在活体动物体内实现腺嘌呤碱基编辑器 (ABE8e) 对致命罕见病克拉伯病致病基因GALC的精准单碱基修复,通过双AAV9载体在新生小鼠脑中高效递送,仅以极低的编辑效率便显著恢复半乳糖神经酰胺酶活性、减少神经毒性物质蓄积、保护髓鞘与神经结构、改善运动功能并延长生存期,且未产生明显脱靶效应、炎症或肿瘤风险,不仅为这一致命性疾病提供了安全有效的根治性新策略,也证实体内单碱基编辑在极低效率下即可逆转严重病理,为中枢神经系统单碱基突变遗传病的 “一次治疗、长期治愈” 奠定了里程碑式的转化基础。