2023年8月22日,诺华宣布PCSK9 siRNA疗法Inclisiran获得NMPA批准上市,作为辅饮食的辅助疗法,用于治疗成人原发性高胆固醇血症(杂合子型家族性和非家族性)或混合型血脂异常患者,商品名为乐可为,至此该药物成为国内首款上市的小干扰RNA(siRNA)药物。

inclisiran(商品名:Leqvio)原本是由MDCO公司和Alnylam合作开发的。2019年,诺华以97亿美元收购The Medicines Company(MDCO公司)获得。Inclisiran是一款first-in-class靶向PCSK9的siRNA药物,每年只需两次皮下给药,该药物是全球首款也是目前唯一一款PCSK9 siRNA降血脂药物。Leqvio在欧美的定价为6500美元/年,约4.7万元/年;国内定价9988元/针,约2万元/年。

2020年12月,inclisiran率先在欧盟获得批准上市,用于治疗成人高胆固醇血症及混合性血脂异常。2021年12月,Inclisiran获得FDA批准上市,用于治疗高血脂,商品名为Leqvio,仅需每年给药两次。2023年8月,该产品在递交新药申请9个月后即在中国获批。
Inclisiran能够与RNA诱导沉默复合体(RISC)结合,并在反义链的介导下与编码PCSK9蛋白的mRNA结合,抑制PCSK9蛋白的产生。从而阻止PCSK9介导的与低密度脂蛋白受体(LDLR)降解,使得能够清除血液中低密度脂蛋白的LDLR的数量增加,从而降低LDL-C水平。
支持Inclisiran最初在欧盟和美国上市的关键性Ⅲ期临床试验共3项:ORION-9、ORION-10和ORION-11。这三项临床研究一共入组了3660名受试者,其中1728名HeFH或ASCVD患者接受了Inclisiran治疗。研究结果已证实,每年仅需皮下注射两针Inclisiran即可长久平稳地降低LDL-C水平,降幅可达50%以上。这些结果已发表在《新英格兰医学杂志》上。[1,2,3]
ORION-8是三项III期试验(ORION-11、ORION-10和ORION-9)和一项II期试验(ORION-3)的开放标签扩展,是迄今为止关于Inclisiran最大规模的临床研究其研究结果已在2023年欧洲心脏病学会年会(ESC 2023)上发表。在这些临床试验中,ASCVD患者或有心血管疾病风险的患者每年接受两次inclisiran,持续三年。当对患者进行长达三年的随访时,78.4%的患者达到了LDL-C目标。Inclisiran还将LDL-C水平降低了49.4%。长期安全性数据与既往结果一致,证实Leqvio疗法具确定且有利的安全性特征[4]。
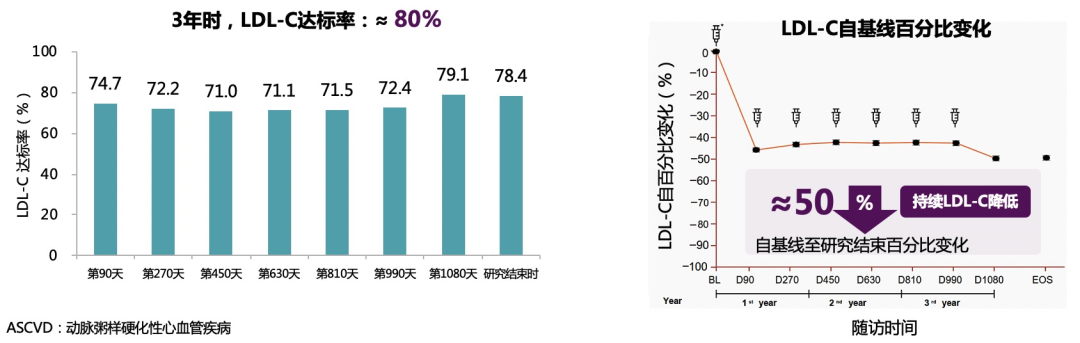
ORION-8 研究中患者LDL-C达标率和降幅
2024年7月18日,诺华发布上半年财报:2024 H1净销售额达243亿美元,营收74亿美元;其中Q2净销售额125亿美元,同比增长11%;营收40亿美元,同比增长47%。其中,中国区Q2净销售额达11亿美元,同比大增27%,公司上调了2024全年财务预期。
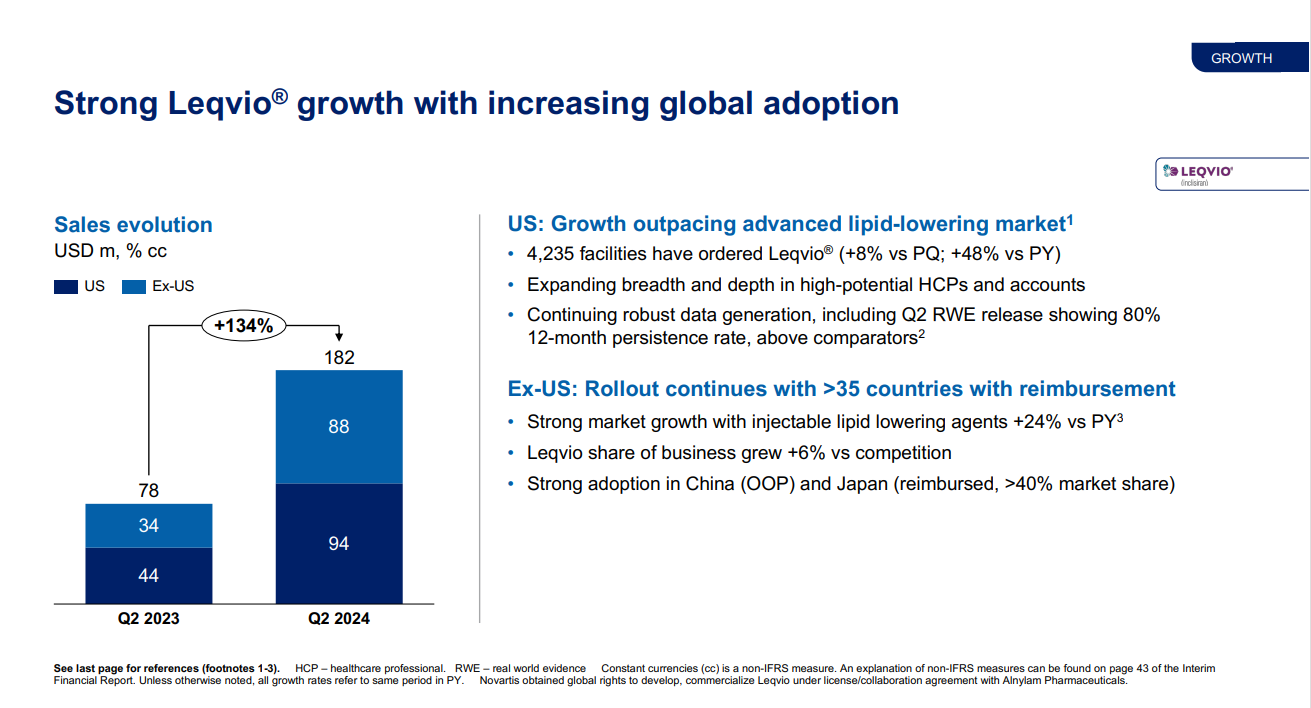
PCSK9 siRNA新药Leqvio 2024 Q2销售额1.82亿美元,同比增长134%,2024 H1销售额为3.33亿美元,已接近2023年全年销售额。2022年Leqvio业绩为1.12亿美元,2023年销售额3.55亿美元。除美国外,在35个国家继续推广。
PCSK9是前蛋白转化酶家族中的第9个蛋白酶K亚家族,主要由肝脏合成的分泌型丝氨酸蛋白酶,可与肝细胞上低密度脂蛋白胆固醇受体( LDL-R) 结合并使LDL-R降解,从而减少LDL-R对血液中LDL-C的清除,升高LDL-C的水平。
国内已批准上市的三款PCSK9抑制剂包括:PCSK9单抗依洛尤单抗(瑞百安,Evolocumab)和阿利西尤单抗(波立达,Alirocumab)以及一款PCSK9 siRNA英克司兰钠注射液(乐可为,Inclisiran)。目前,国内多家企业看好靶向PCSK9 siRNA药物的巨大市场及研发空间,并开发出多款在研药物:

1、圣因生物:SGB-3403
圣因生物核心产品SGB-3403已在中国和澳大利亚进入临床试验阶段,正在稳步推进单剂量爬坡试验。SGB-3403是一种靶向肝细胞PCSK9的siRNA-GalNAc结合物,采用了圣因生物的新一代GalNAc偶联技术递送到肝脏细胞,通过RNAi抑制肝脏PCSK9蛋白的合成。SGB-3403临床上拟开发用于高胆固醇血症、混合型血脂异常以及动脉粥样硬化性心血管疾病的治疗,以降低心血管事件的风险。
2、靖因药业:SRSD101注射液
3月22日,靖因药业宣布其自主开发的特异性肝靶向PCSK9小核酸药物SRSD101注射液1期临床研究已顺利完成全部受试者入组给药,安全性、耐受性良好,暂无不良事件。这是一项随机、双盲、安慰剂对照的单剂量递增的临床研究,旨在评价SRSD101的安全性、耐受性、药代动力学和药效学特征。
SRSD101注射液正是该公司研发的双链小干扰核酸(siRNA)药物,其特异性肝靶向前蛋白转化酶枯草溶菌素9(PCSK9)的mRNA, 阻断PCSK9的蛋白合成,从而增强肝细胞摄取LDL-C能力来实现降血脂的作用。临床前研究显示,SRSD101兼具强效持久降脂疗效和良好的安全性,有望成为新一代的降血脂产品。该产品已在中国获批临床,拟开发治疗原发性高胆固醇血症。
3、石药集团:SYH2053注射液
2023年11月30日,石药集团宣布SYH2053注射液(双链小干扰RNA(siRNA)药物)国内获批开展临床试验。该产品是一款通过GalNAc实现肝脏靶向递送的PCSK9 siRNA药物,用于治疗成人原发性高胆固醇血症或混合型血脂异常。临床前研究显示,该产品的药物活性作用时间明显长于同类型siRNA产品,并具有良好的安全性,极具临床开发价值。该产品亦是集团首个获批临床试验的siRNA产品。
4、大睿生物:RN0191注射液
2023年12月29日,大睿生物首款自主研发的RN0191注射液已成功获得中国国家药品监督管理局批准的临床试验申请默示许可。作为第三个进入中国和海外同步临床开发的PCSK9 siRNA,该产品可用于治疗高胆固醇血症、混合型高脂血症以及动脉粥样硬化性心血管疾病,以降低心血管事件发生的风险。
2023年6月,RN0191在澳洲获得伦理批准开展首次人体试验。目前该实验进展顺利,现有数据表明RN0191耐受性和安全性良好,并显示出了剂量依赖性的药效和疗效。同时,多个重要脂代谢的指标,包括脂蛋白(a)的下降也非常显著,进一步证实了其显著双重降低低密度脂蛋白和脂蛋白(a)的潜在优势。这一结果为该差异化产品后续临床试验的开展提供了有力支持。
5、瑞博生物:RBD7022
瑞博生物基于其自主创新的RIBO-GalSTAR肝靶向递送技术而开发的一款旨在治疗高血脂症的GalNAc缀合siRNA药物RBD7022,目前处于I期临床研究阶段。2023年12月,齐鲁制药以超过7亿元人民币获得RBD7022在大中华区(中国大陆、香港及澳门)的开发、生产和商业化权利。
RBD7022通过抑制PCSK9蛋白的表达,减少低密度脂蛋白受体(LDL-R)溶酶体降解,降低血液中LDL-C水平,用于家族性高胆固醇血症及经他汀治疗后LDL-C仍不能被很好控制的动脉粥样硬化性心血管疾病(ASCVD)患者。已有的研究数据显示,RBD7022具有良好的安全性和耐受性,降脂效果显著,有望实现数月甚至更长周期的给药间隔,极大地提高患者的依从性。
参考资料:
[1]Raal, F. J., Kallend, D., Ray, K. K., Turner, T., Koenig, W., Wright, R. S., ... & Kastelein, J. J. (2020). Inclisiran for the treatment of heterozygous familial hypercholesterolemia.New England Journal of Medicine, 382(16), 1520-1530.
[2] Ray, K. K., Wright, R. S., Kallend, D., Koenig, W., Leiter, L. A., Raal, F. J., ... & Kastelein, J. J. (2020). Two phase 3 trials of inclisiran in patients with elevated LDL cholesterol.New England journal of medicine, 382(16), 1507-1519.
[3]Zhang L, Wang Z, Fang J, et al. Final overall survival data of sintilimab plus pemetrexed and platinum as First-Line treatment for locally advanced or metastatic nonsquamous NSCLC in the Phase 3 ORIENT-11 study. Lung Cancer. 2022;171:56-60. doi:10.1016/j.lungcan.2022.07.013.
[4]Wright RS, Raal FJ, Koenig W et al. ORION-8: Long-term efficacy and safety of twice-yearly inclisiran in high cardiovascular risk patients. Presented at ESC Congress 2023, Amsterdam, The Netherlands (25-28 August). Late-breaking science on pharmacology.
[5]诺华财报