国内首个戈谢病基因治疗产品LY-M001注射液临床I期试验招募已启动
基因治疗将为戈谢病患者带来什么改变?
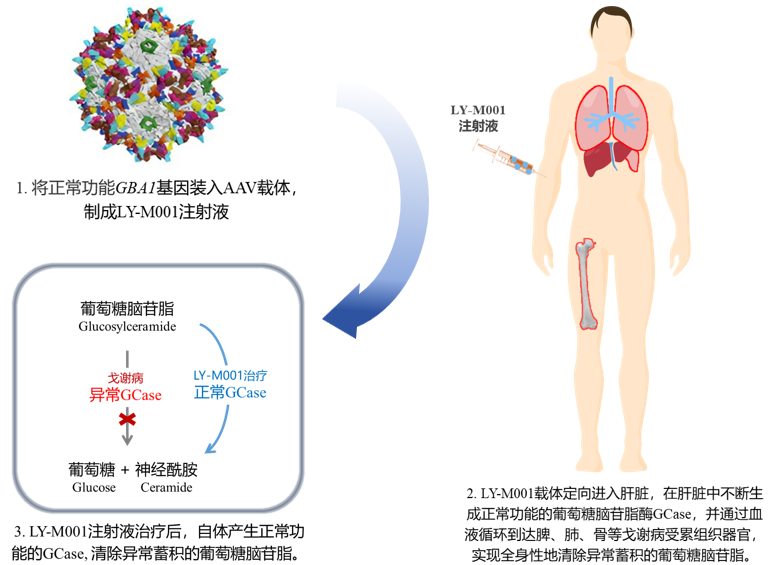
戈谢病是一种由于GBA1基因变异,导致葡萄糖脑苷脂酶功能缺陷,进而引起体内有害代谢底物大量累积引发的疾病。患者发生肝脾肿大、贫血、血小板减少、骨痛、神经系统症状等。目前患者能获得的特异性治疗包括ERT治疗(伊米苷酶)和SRT治疗(艾格司他),但在这些治疗方案下,患者不得不接受频繁给药,甚至要面临长期用药后疗效降低,病痛仍然逐步进展的风险。同时,现有药物高昂的价格给患者和家庭带来沉重的负担。
基因治疗顾名思义就是从基因缺陷这个根本病因上解决问题。对于戈谢病而言,就是将正常功能的GBA1基因通过载体递送入患者体内。患者只需接受一次给药,就能获得长期稳定产生正常功能葡萄糖脑苷脂酶(GCase)的能力,从根本上恢复健康。那么,怎么将GBA1基因送入人体呢?答案就是——AAV载体!
AAV怎么治疗I型戈谢病?
AAV是临床治疗应用最为广泛且最安全的基因治疗载体,它就像一辆运输车,可以载上基因运送到特定的组织细胞中,到达目的地的治疗性基因可长期稳定地发挥作用,而AAV载体在任务完成后便功成身退,自然降解。目前,在欧洲、美国等地区,已有8款使用AAV作为载体的基因治疗药品被批准上市,用于治疗遗传性罕见病。
如何获得基因治疗的机会?
1、 看诊断报告,确认是戈谢病I型患者就来联系我们吧!
2、根据提示提交诊断报告,等待专家审核后与您联系。
3、按照沟通好的时间,去中国医学科学院血液病医院(天津,可获得适当交通补贴),我们会为您联系张凤奎教授领导的专家团队,免费为您进行检查和治疗。
药品信息
LY-M001是国内首个针对戈谢I型的AAV基因治疗药物,已完成中国和美国IND申报且均已获批,并获得FDA孤儿药资格认定。
目前,LY-M001的IIT临床研究正在进行中,已经入组的3例受试者输注后均体现出良好的耐受性,且均未发生严重不良反应,同时体现出稳定的葡萄糖脑苷脂酶高效表达能力及有害底物清除能力,治疗过程中未发现针对目标蛋白的抗药抗体(ADA)产生。
入组条件
本研究全称“一项评估LY-M001注射液治疗I型戈谢病成人患者的安全性、耐受性和有效性的多中心、开放、单臂、单次给药、剂量递增和扩展的I/II期临床研究”(方案号:LY-M001-GD-101)。如果您或您周围有符合下列条件的患者,请联系我们:
1、年龄≥18周岁,且≤60周岁,性别不限。
2、由实验室检测确认具有葡萄糖脑苷脂酶基因(GBA1)等位基因双突变且葡萄糖脑苷酯酶活性降低至正常值的30%以下(如干血试纸法DBS<1.19mmol/L/h),并满足戈谢病(GD)临床诊断标准的戈谢病I型(GD1)患者。
3、符合以下a)或b)的患者
a)经治的戈谢病I型患者,若既往接受过GD的酶替代疗法(ERT)或底物清除疗法(SRT),需治疗6个月以上,在给药前洗脱5个药物半衰期及以上,或由研究者综合判断患者病情稳定。
b)初治或未进行治疗的GD1患者,筛选时符合以下一项或多项:
· 血红蛋白≥80g/L且小于正常值下限;
· 血小板≥40×109/L且小于正常值下限;
· 肝肿大;
· 脾肿大。
注:需由研究者综合判断初治或未进行治疗的患者病情稳定适合入组,系统性受累严重的患者谨慎入组。
4、生育能力的女性(WOCBP)受试者妊娠试验阴性。
5、受试者及其伴侣在筛选期至研究结束后6个月内无生育计划、且自愿采取有效的避孕措施者(如禁欲、避孕套等);受试者无捐献精子或卵子计划。
6、受试者在研究期间及研究结束后至少1年内不得献血。
参与本次临床试验您将获得
经研究医生判断,如果您符合本研究的入选条件并自愿参加,您将获得:
1、本次临床试验相关检查费和治疗费免费;
2、适当的交通、营养补助;
3、专业研究医生的病情指导。
研究期间,将密切监测您的健康及安全,我们的筛选流程旨在确保您适合参加本研究。
是否参加完全取决于您的意愿。如果您有意参加,请与研究医生联系,他(她)将向您详细介绍本研究概况及您需要配合事项,并初步判断您是否符合入选要求,即使您不愿意参加本研究,也不会受到任何对您不利的影响,并对您的相关信息进行保密。最终是否能成功参加本研究取决于研究者的判断。您的健康是我们共同的目标和期盼,同时也感谢您对医学科学的进步作出贡献,我们期待您的参加。
如您想详细咨询或参加本项目,请联系:
联系人:临床协调员
联系电话:19121572057