辉瑞(Pfizer)近日宣布,美国FDA已批准其所开发的一次性基因疗法Beqvez(fidanacogene elaparvovec)用于治疗18岁或以上中度至重度血友病B成人患者,这些患者正在接受凝血因子IX(FIX)预防治疗,或目前或过去有危及生命的出血,或反复发生严重的自发性出血事件。这些患者体内经美国FDA批准的检测未侦测到靶向腺相关病毒血清型Rh74var(AAVRh74var)衣壳的中和抗体。

血友病B是一种危及生命的退行性疾病,患者由于基因出现突变,导致缺乏凝血因子IX。患有该疾病的患者容易发生关节、肌肉和内脏器官出血,出现疼痛、肿胀和关节损伤。目前的治疗包括终生每周或每月多次定期静脉输注凝血因子IX,一年可能需要进行超过一百次以上的治疗,以暂时替代或补充低水平的凝血因子。

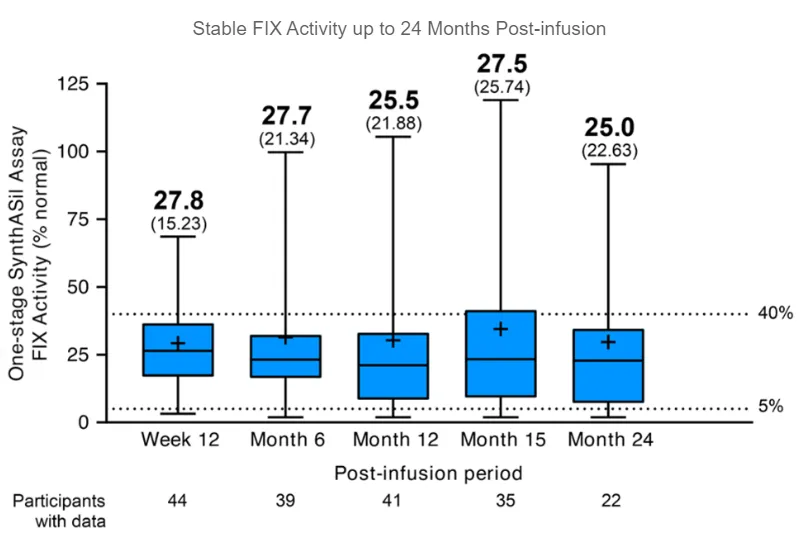
美国FDA批准Beqvez主要是基于单组、开放标签临床3期试验BENEGENE-2的结果,该研究旨在评估Beqvez治疗中重度至重度血友病B(定义为凝血因子IX循环活性≤2%)成年男性受试者(18-65岁)的疗效和安全性,此试验共有45名患者入组。分析显示,BENEGENE-2试验达到其主要终点,即与FIX预防性治疗方案相较,患者在经过Beqvez输注后,其总出血事件的年化出血率(ABR)达到非劣效性与优效性。根据辉瑞2022年12月所公布的BENEGENE-2积极数据,该基因疗法使患者的ABR降低了71%,年化凝血因子输注率降低了92%。
该治疗总体上也是安全的,没有导致死亡或血栓事件。BENEGENE-2记录了14起严重不良事件,其中两起被认为与基因治疗有关。
Beqvez是一种新型的在研基因疗法,含有生物工程化的腺相关病毒衣壳和FIX基因的高活性变体。对于血友病B患者来说,这种基因治疗的目标是使他们能通过一次性治疗产生自体的FIX蛋白,而非像目前的标准治疗那样需要定期静脉输注FIX。辉瑞于2014年12月以2000万美元预付款从Spark Therapeutics获得Beqvez。加拿大卫生部(Health Canada)于今年1月批准Beqvez上市,目前欧洲药品管理局(EMA)正在进行该疗法的审评。
除了Beqvez,辉瑞目前还有另外两款基因疗法giroctocogene fitelparvovec与fordadistrogene movaparvovec处于临床3期试验阶段,分别用以治疗血友病A和杜氏肌营养不良(DMD)患者。此外,辉瑞也正在进行一项3期试验,检视其在研组织因子途径抑制单抗marstacimab用于治疗体内存有(或无)凝血因子抑制物的血友病A和B患者。目前美国FDA与EMA正在审评marstacimab的上市许可申请。
近年来,FDA生物制品评价和研究中心(CBER)批准的基因疗法和细胞疗法总数量从2020年的1款迅速发展到2021年的4款,2022年的5款和2023年的7款。在2020至2023年期间所获批的17款细胞和基因疗法之中,16款用于治疗罕见病,占比高达94%。
获批治疗非癌症罕见病的细胞和基因疗法集中在2022至2023年间,包括两款分别用于治疗血友病A和血友病B的基因疗法Roctavian(valoctocogene roxaparvovec)和Hemgenix(etranacogene dezaparvovec)。Beqvez是FDA所批准的第二款用以治疗血友病B患者的基因疗法。
参考资料:
[1] U.S. FDA Approves Pfizer’s BEQVEZ™ (fidanacogene elaparvovec-dzkt), a One-Time Gene Therapy for Adults with Hemophilia B. Retrieved April 26, 2024 from https://www.pfizer.com/news/press-release/press-release-detail/us-fda-approves-pfizers-beqveztm-fidanacogene-elaparvovec