1月11日,Acorda Therapeutics宣布收到渤健(Biogen)的终止合作书函,涉及多发性硬化症药物Fampyra(fampridine)的全球商业化权益。退还协议将于2025年1月1日生效,这也意味着两家公司长达15年协议的终止。
Acorda表示,随着各地区上市许可转让和分销安排的敲定,他们将于今年开始承担起商业化责任。

Acorda和渤健的合作协议始于2009年7月,后者以5.1亿美元的总交易额(首付款1.1亿美元)获得了fampridine在美国以外的开发和商业化权益。彼时,fampridine的上市申请正在接受FDA的审查。
2010年1月,fampridine顺利在美国获批上市,商品名为Ampyra,适用于改善多发性硬化症 (MS) 患者的步行能力。一年后,该药物在欧盟获有条件批准上市,商品名为Fampyra。2021年,fampridine进入中国市场。
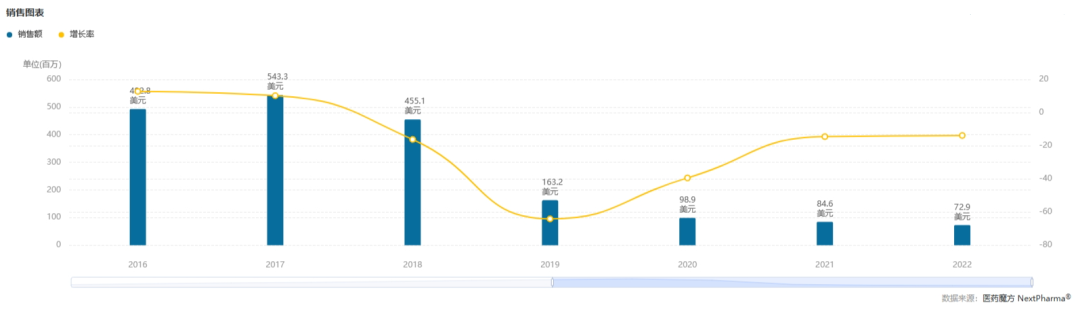
上市当年,Ampyra便为Acorda创造了1.41亿美元的收入。此后7年,Ampyra的销售额一路走高,在2017年达到了5.433亿美元。不过,这种势头在2018年受到了打击,因其多项专利被判无效,导致仿制药得以提前进入市场参与竞争。Acorda也因此裁去100名员工,以降低可预见的公司收入下降所带来的资金紧张威胁。2022年,Ampyra的销售额已下滑至7290万美元。
MS是一种累及中枢神经系统的终身性、进展性的自身免疫疾病,中枢神经系统受累逐渐引起肢体残疾, 动、视觉和认知等神经系统功能。MS患者可出现广泛多样的神经功能缺损,包括步行能力障碍、疲乏、痉挛状态、共济失调、疼痛、震颤和无力。由于对运动、感觉、视觉、小脑和前庭功能系统进行有效协调,因此步行能力障碍是MS的一个关键不良特征。高达85%的MS患者将步行障碍视为他们的初始 因此MS患者和神经科医生均认为步行障碍对正常日常功能和总体生活质量产生最大的不良影响。