什么是ADA-SCID及其应用
腺苷脱氨酶缺乏导致的SCID是在重症联合免疫缺陷疾病中排在第二大类的免疫缺陷疾病,占SCID的10%~20%。
ADA(腺苷脱氨酶)-SCID患者通常有以下表现,如免疫系统受损:由于患者体内的免疫系统具有严重的缺陷,该类型疾病的患者表现往往发生在患者出生一年内,伴有严重感染和生长发育障碍。
出生时,由于母体IgG可穿越胎盘屏障给胎儿,患儿总免疫球蛋白水平在出生时可能表现正常或略低于正常值,但当来源母体的IgG水平下降时,明显的免疫缺陷的症状就会表现出来。如持续性腹泻、皮炎和严重感染。浅表淋巴结与扁桃体难以触及及发现,胸部影像学检查无法检测到胸腺等免疫器官。
腺苷脱氨酶的缺乏可使T淋巴细胞因代谢产物的累积而死亡,究其病因,腺苷脱氨酶的缺乏是由于腺苷脱氨酶(ADA)基因缺失引起,腺苷脱氨酶基因位于20q13-qter,该基因负责编码一条含363个氨基酸残基的多肽链。
ADA在人体中负责催化腺苷酸和脱氧腺苷酸的脱氨基,腺苷脱氨酶的缺乏会让代谢中产生的若干废物堆积,导致细胞中ATP的耗尽,进而导致T和B等淋巴细胞死亡,从而破坏免疫系统,引发SCID。该类型的患者的症状可能过注射ADA得到一定程度的缓解,但该药物价格不菲,该疾病也可以通过骨髓移植来治愈,但找到能够匹配的骨髓捐献者是非常困难的事情。
数十年来,科学家一直在为攻克这一疾病而进行努力。

图为《Blood》杂志论文标题
(来源:Long-term outcomes after gene therapy for adenosine deaminase severe combined immune deficiency. Blood (2021) 138 (15): 1304–1316.)
改造干细胞的治疗基因疗法
在2021年,世界著名医学期刊 《Blood》报道了一种基因疗法,该疗法是首先从患儿骨髓中提取出造血干细胞,然后通过病毒载体将正常拷贝的ADA基因导入干细胞,再将改造后的干细胞回输患儿体内,以产生并持续供应能够抵抗感染的健康免疫细胞,该疗法在2009-2012年期间,共有10名患儿接受该疗法。
结果显示,其中9名患儿情况持续保持稳定,在后续几年中无需其他治疗方法支持其免疫系统。研究人员指出,参与研究的10名患儿基本为婴儿,仅一名年龄为15岁,也是唯一一名没有通过治疗显著获益的患儿,这表明该疗法在年龄较小的儿童中效果更明显。
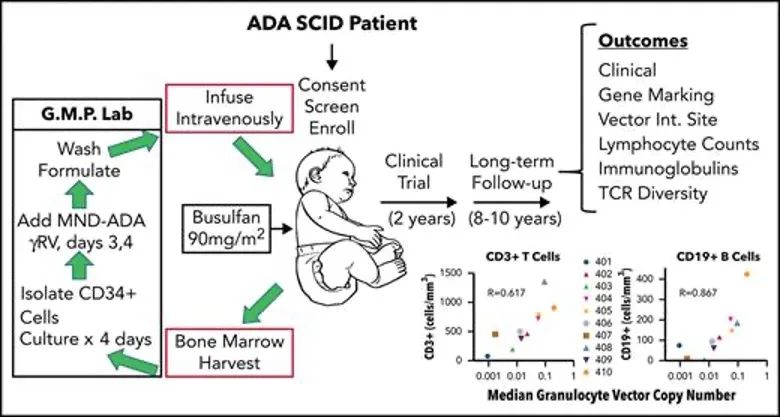
图为该研究示意图(来源:Long-term outcomes after gene therapy for adenosine deaminase severe combined immune deficiency. Blood (2021) 138 (15): 1304–1316.)
同年,世界著名医学期刊 《新英格兰医学杂志》报道了一种相似的基因疗法。该疗法治疗了50名患有ADA-SCID的患者(其中30名在美国,20名在英国),该研究在体外对自体造血干细胞和祖细胞转导可以编码人ADA的自身失活慢病毒载体。

图为发表于《新英格兰医学杂志》的论文题目
(来源:Autologous Ex Vivo Lentiviral Gene Therapy for Adenosine Deaminase Deficiency. NEJM 384;21 nejm.org May 27, 2021)
在接受试验的2~3年后,参与该临床研究的患儿都存活了下来,并健康状况良好,48位患儿已完全没有了ADA-SCID症状,只有两位仍在进行长期观察。其中一位进行了骨髓移植,这也证明了该治疗后,患儿仍然能回到正常的治疗方法中。
该疗法的诞生预示越来越多疾病进入基因治疗范畴。随着基因治疗的发展与井喷,会有越来越多疾病随之而被攻克。