导语
Usher综合征 (Usher syndrome, USH) 又称遗传性视网膜色素变性-感音神经性耳聋综合征,分为USH1,USH2和USH3三种临床类型,主要表现为不同程度的视网膜色素变性和感音神经性耳聋,伴或不伴前庭功能障碍。MYO7A基因是第一个被发现的USH1致病基因,其突变将产生Usher综合症1B亚型 (USH1B)。
近日,在刚刚结束的2025年欧洲视网膜专家学会(EURetina 2025) 年会上,AAVantgarde Bio公司公布了其用于USH1B创新基因疗法AAVB-081的最新临床数据。初步结果不仅验证了其独特的双AAV载体平台的安全性与潜力,更在视力改善方面展现出积极信号,为长久以来缺乏有效治疗手段的Usher 1B患者群体带来了新的希望。
|AAVantgarde双AAV平台再显锋芒
在刚刚结束的2025年欧洲视网膜专家学会 (EURetina 2025) 年会上,AAVantgarde Bio公司公布了其用于USH1B创新基因疗法AAVB-081的最新临床数据。初步结果不仅验证了其独特的双AAV载体平台的安全性与潜力,更在视力改善方面展现出积极信号,为长久以来缺乏有效治疗手段的Usher 1B患者群体带来了新的希望。

AAVantgarde官网截图
MYO7A基因是第一个被发现的USH1致病基因,位于染色体11q13.5区域,含49个外显子,编码2215个氨基酸,其突变将产生Usher综合症1B亚型 (USH1B),导致患者出生时失聪,并在生命早期伴随进行性视力丧失,最终可能导致失明。由于MYO7A基因长度达到6.7 kb,超出了传统AAV载体的包装极限,这使得USH1B的基因治疗面临巨大挑战。
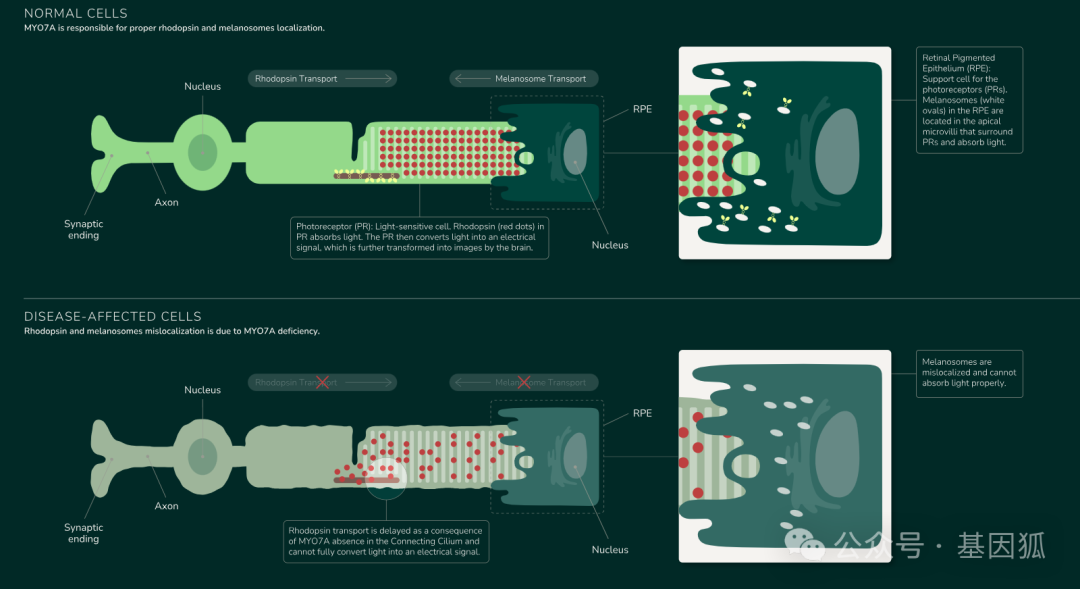 AAVB-081作用机理
AAVB-081作用机理
AAVantgarde凭借其创新的双AAV载体平台,成功将过长的MYO7A基因分装到两个AAV载体中,通过视网膜下给药,使其在靶细胞内重组表达,从而实现基因修复。这一创新性技术路径,是实现超大基因高效体内递送的关键,也体现了基因治疗载体工程的最新突破。
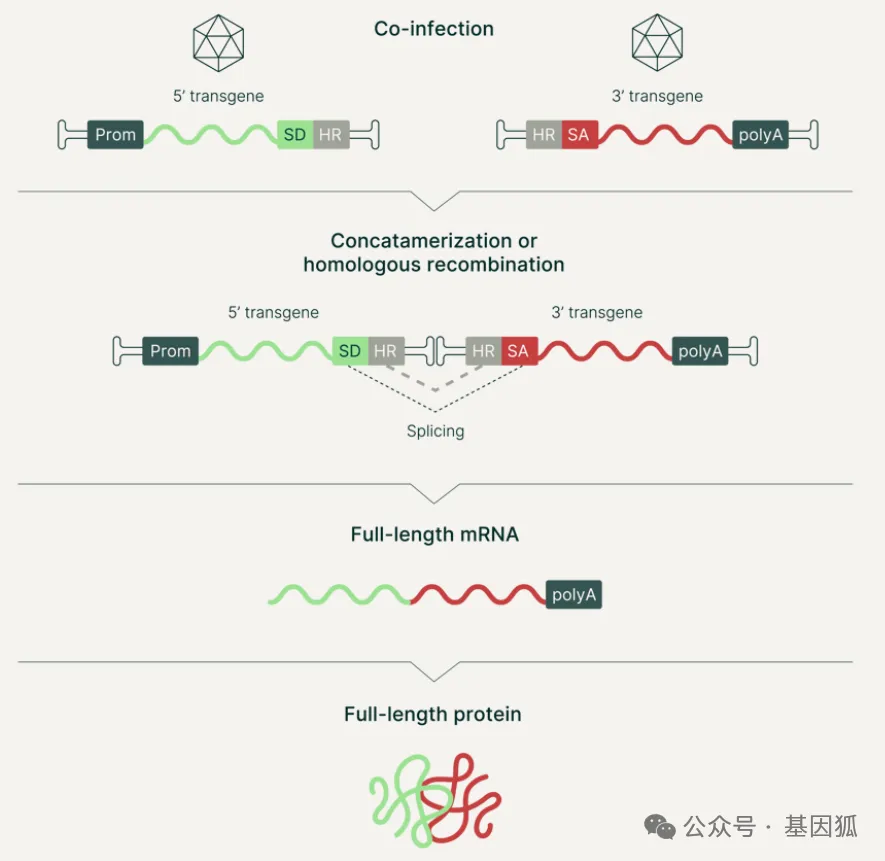 AAVantgarde公司Dual Hybrid技术平台
AAVantgarde公司Dual Hybrid技术平台
|LUCE-1试验:安全为先,疗效初显
此次公布的LUCE-1研究 (NCT06591793) 是一项多中心、开放标签、剂量递增的1/2期临床试验,旨在评估玻璃体腔注射AAVB-081在USH1B视网膜色素变性患者中的安全性、耐受性及初步疗效。此次公布的数据,集中于前11名接受治疗的患者的安全性,以及前4名随访期≥180天(其中首例患者随访已达1年)患者的初步疗效。
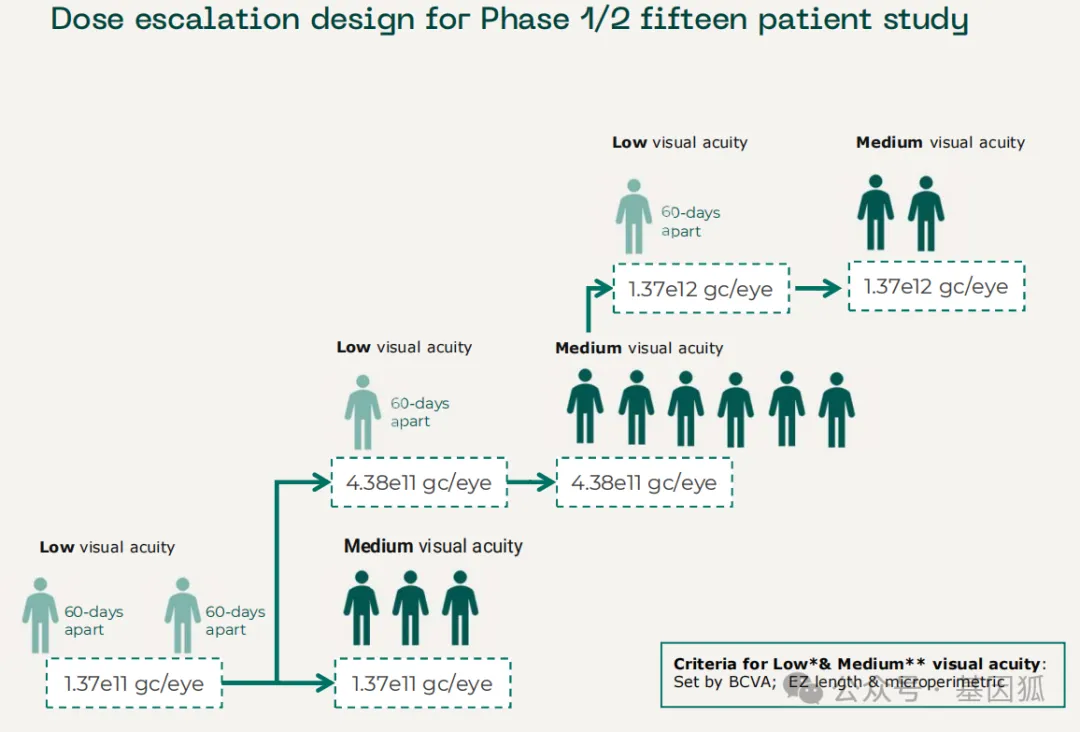 LUCE-1研究剂量递增设计
LUCE-1研究剂量递增设计