最新发布的研究表明,与同期未接受治疗的患儿相比,在接受美国FDA批准的杜氏肌肉萎缩症(DMD)基因疗法SRP-9001治疗4年后,患儿仍然持续保持肌肉运动功能。研究人员指出,依据DMD自然病史预计肌肉功能衰退的年龄段,仍然保持肌肉运动功能的长期持续稳定,这在临床上是很有意义的。此外,SRP-9001治疗后4年的安全性良好。
作为评估SRP-9001基因疗法的几个研究团队之一,俄亥俄州立大学儿科神经病学教授杰里·门德尔博士领导的研究团队评估了4名4-8岁接受一次静脉输注治疗的男性儿童患者的数据,在刚刚结束的2023年美国神经肌肉电诊断医学协会(AANEM)年会上发表。

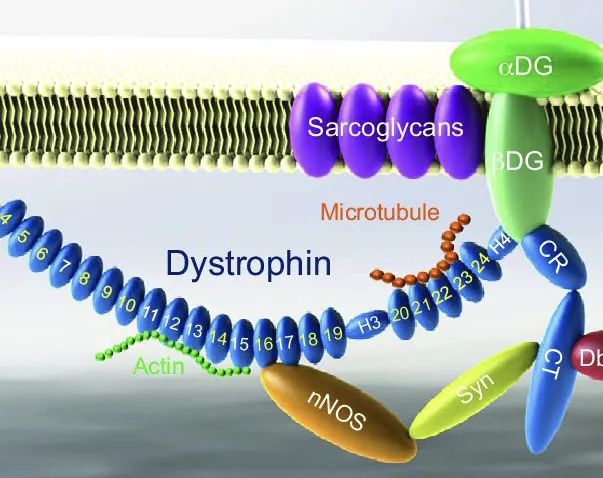
DMD被认为是最严重的肌肉萎缩症之一,它会导致进行性肌肉消耗,根本原因是一种遗传基因缺陷。SRP-9001是一种静脉输注的单剂量重组基因疗法,旨在提供一种剪辑后的dystrophin,以弥补这种基因缺陷。
2023年6月,基于腺相关病毒载体(AAV)的SRP-9001基因疗法获得了美国食品药品监督管理局(FDA)的加速批准,用于治疗4-5岁患有DMD并确诊有基因突变的儿科患者。
SRP9001疗法以每公斤体重133万亿个载体基因组剂量,经静脉输注,持续1-2小时。所有患者输注前1天和输液后30天,给予强的松1mg/kg治疗。
在治疗4年后,没有新的不良事件发生。所有与治疗相关的不良事件主要发生在治疗后70天内,并且都得到了解决。
基因疗法最常报告的不良反应包括呕吐、恶心、肝酶增加、发热和血小板减少,所有这些都发生在SRP9001输注后90天内,并且是可以控制的。
在血液生化检测随访中,没有观察到严重的生化指标异常。3名患者在治疗后的3个月内,γ-谷氨酰转肽酶升高,通过口服类固醇治疗后都得到解决。其他报告的不良事件包括急性严重肝损伤、免疫介导的肌炎和心肌炎。由于后一种风险,该疗法禁止DMD基因中外显子8和/或外显子9缺失的患者纳入到该基因疗法临床研究。
进一步探索性分析表明,与21名未接受治疗的DMD患者外部队列相比,接受SRP-9001的患者在NSAA评分的最小平方平均值变化存在9.4个点的统计学显著差异(P = .0125)。在关键上升时间、4级爬升以及10米和100米步行/跑步功能测试方面,相比基线均有类似的改善趋势。
迄今为止,已报告的80多名患儿接受SRP-9001的临床试验结果表明,其临床有效和安全方面是一致的。
SRP-9001是一种基于AAV载体的基因疗法,根据FDA加速批准途径获得批准,需要继续在3期EMBARK研究(NCT05096221)中加强对该药物的有效性观察。该研究将于2023年底完成,并于2024年初宣布数据。
SRP-9001与其他基因疗法的共同问题是治疗成本高,在200-300万美元之间。纽约罗切斯特罗切斯特大学医学中心神经学和儿科教授Emma Ciafaloni医学博士强调,需要考虑批准与获得基因疗法,以及如何优化获得创新疗法的机会。需要考虑成本是多少,如何获得它,以及是否有可持续的模式。她还指出,我们需要考虑如何在更广泛的层面上做得更好,因为这不是供应商问题或制造商问题,而是社会问题。