2022年11月,罗氏合作伙伴Sarepta Therapeutics公司宣布,其AAV基因疗法SRP-9001的上市申请已经获得FDA受理和优先审查,FDA预计于2023年5月29日前公布审评结果。

而近期,Sarepta在其2022年报表示,其AAV基因疗法SRP-9001 BLA过程中不需要经过FDA咨询委员会环节。FDA对SRP-9001进行了中期审查,询问了有关化学、制造和控制的问题,表示不打算举行FDA咨询委员会,PDUFA日期为5月29日。这意味着该款基因疗法已经得到了监管部门的初步认可,距离上市再进一步。
据悉,SRP-9001是一款针对DMD(杜氏肌营养不良症)的AAV基因疗法,通过将目的基因递送到肌肉组织,针对性地产生抗肌萎缩蛋白的有效成分。其三项临床试验结果显示,在80多名接受治疗的患者中,SRP-9001治疗在多个时间点显示出积极的结果(包括治疗后一年,两年和四年),此外还表现出了一致的安全性。
DMD是一种以进行性肌肉无力为特征的罕见致命性神经肌肉遗传病,患者一般在2~5岁时开始发病,20岁左右因心肌衰竭而死亡。据统计,全球平均每3500个新出生的男婴中就有一个患有杜氏肌营养不良。同时拥有罕见与遗传的两大特性,使得DMD更加难以治疗,药物研发也一度陷入困境,虽然目前已经涌现了一些资料手段,但仍然缺乏十分有效的治疗方法,而基因疗法给这种疾病带来了新的希望。
回顾该款基因疗法的进展历程,从2017年四季度首次IND获批,到现在距离上市只差临门一脚,SRP-9001临床试验做了5年,消耗了数十亿的资金。一路走来,Sarepta曾面临来自辉瑞和Solid Biosciences的竞争以及临床失败的威胁,但目前后两家的临床进度已经落后于Sarepta。这些充分印证了基因疗法拓荒者的不易,同时也印证了基因疗法治疗难治性疾病的潜力。
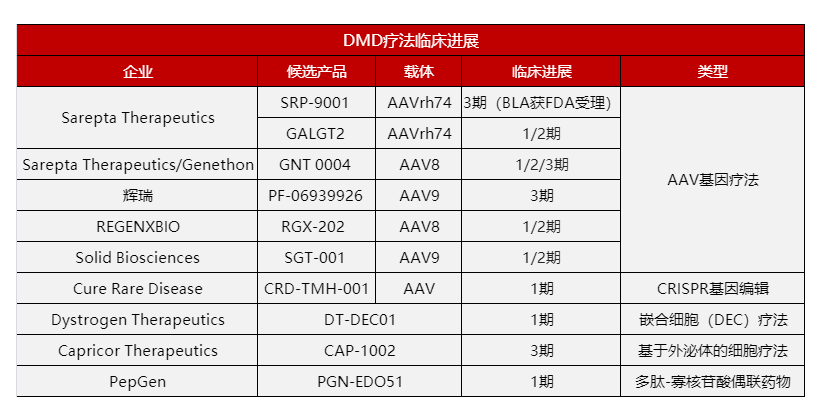
治疗DMD的多种创新疗法及进展
总的来看,该款基因疗法或将于近期迈入商业化,继而填补DMD基因疗法领域的空白。而在国内,国产基因疗法也即将迎来商业化时代。纽福斯首款眼科基因治疗药物NR082已完成中国III期临床试验全部患者入组,经过二十年砥砺发展,国产AAV基因疗法走到了商业化前夕。
参考资料:
1.https://endpts.com/sarepta-wont-need-fda-adcomm-boosting-duchenne-gene-therapys-odds/
版权声明:本网站所有注明“来源:罕见病信息网”的文字、图片和音视频资料,版权均属于罕见病信息网网站所有。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。