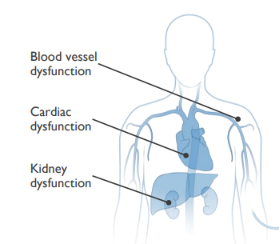
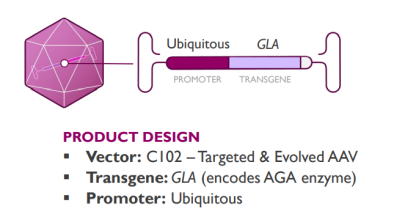
近日,FDA叫停了4D Molecular Therapeutics用于治疗Fabry disease(法布雷病)的基因疗法4D-310的临床试验。 日前,4D公司已经暂停了4D-310项目的患者招募,原因是在两项试验中的前6例患者有3例出现非典型溶血尿毒综合征(aHUS),一种可导致肾脏和其他器官的小血管出现血栓的疾病,尽管所有aHUS症状均在2~4周内得到解决,但有1例69岁的潜在肾功能不良患者发生4级剂量限制性毒性事件,需要进行临时血液透析。 4D公司在确认所有6名患者的长期临床数据可用后,将于今年下半年重新评估Fabry项目。同时将在2月底举行的世界研讨会上分享更多有关4D-310安全性、有效性和心脏活检数据。 Fabry disease(法布雷病)是一种因编码α-半乳糖苷酶A(α-GalA) 的GLA基因突变引起的遗传性疾病。患者由于无法正常代谢鞘氨醇三聚己糖苷(Gb3),致使Gb3在心脏、肾脏和血管等关键器官中积聚,进而引发看危及生命的肥厚型心肌病、心力衰竭、心律失常、肾功能障碍和脑血管等疾病。 法布雷病症状 4D-310是4D公司在研的一种AAV基因疗法,通过使用靶向和优化的AAV载体来递送GLA基因的功能拷贝,通过静脉注射给药,在靶组织中产生高活、稳定的α-GalA。 4D-310产品设计 FDA表示,虽然4D的提前进行了临床暂停,但已经要求其继续对所有服用4D-310的患者进行长期随访。此外,监管机构将继续保持该项目IND申请的开放性和有效性。 Ref 1、4D’s Fabry Gene Therapy on Ice After FDA-Mandated Pause | BioSpace 2、4DMT PPT Template (4dmoleculartherapeutics.com) 3、4D Molecular Therapeutics Announces First Patient Dosed in (globenewswire.com)