肌萎缩侧索硬化症(ALS),俗称“渐冻症”,是一种罕见进行性神经退行性疾病,主要影响皮层、脑干和脊髓中的运动神经元,最终导致活动能力、肌肉控制能力、语言能力以及呼吸能力丧失。据统计,在全球预估有16.8万人罹患此病。
大多数ALS病例是散发性的,但在少数ALS患者群体中,表现出了明显的家族遗传特点,指示ALS可能与特定基因有关。迄今为止,已有近30个基因被证实与ALS的发病相关,最常见的致病基因突变主要包括SOD1、TARDBP、FUS、OPTN、SQSTM1、DAO、DCTN1、VAPB、SIGMAR1、GRN、C9orf72等。但目前业界对ALS的病理生理学还缺乏清晰的认识,猜测其发病机制或与奋性氨基酸毒性、氧化应激损伤、线粒体异常、基因突变、蛋白质失稳和神经营养因子缺乏等有关。
基于病理复杂性等限制因素,ALS还尚无法治愈,并且患者面临的选择也十分之有限。据不完全统计,迄今为止,FDA只批准了三种治疗ALS的药物(Relyvrio、利鲁唑和依达拉奉),但这些药物仅能延缓ALS病情进展,无法彻底治愈ALS。
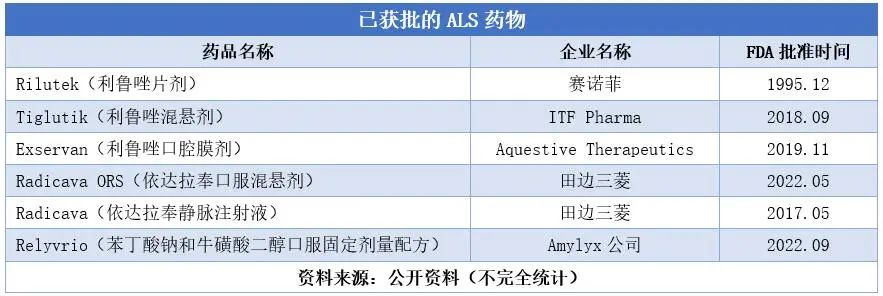
获批治疗ALS的药物(图源:参考资料1)
据统计,近几年有效ALS药物的市场份额呈逐年增长的趋势。根据Grand View Research的一份新报告,2018年全球ALS治疗市场规模约为5.4亿美元,预计到2026年将达到8.9亿美元,2019-2026期间复合年增长率将为5.8%。
近几年随着细胞与基因治疗技术的发展,有不少企业将这种新的治疗模式应用于ALS的治疗,并且取得了积极的进展,最快已步入临床3期。
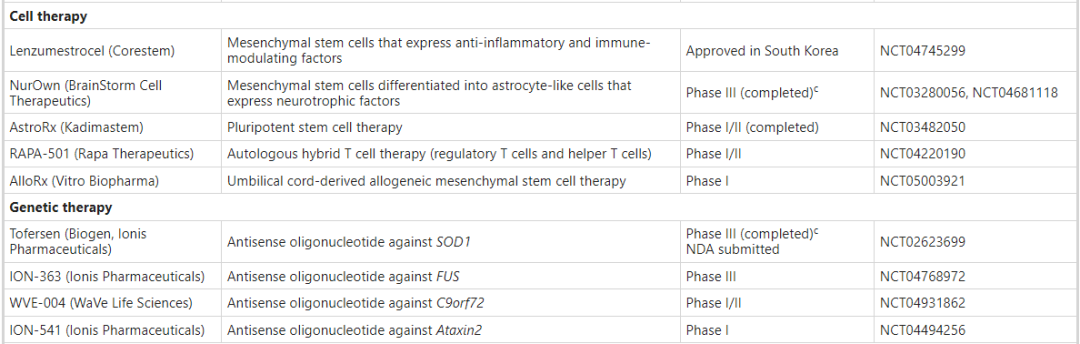
治疗ALS的细胞与基因疗法
(图源:参考资料2)
干细胞疗法
◆ BrainStorm Cell Therapeutics:NurOwn
NurOwn是一款自体干细胞疗法,源自于患者自身骨髓的间充质干细胞,在体外采用分化培养基诱导下定向分化为能分泌神经营养因子(NTF)的MSC-NTF细胞。经修饰后的MSC-NTF细胞回输到患者体内,可以有效地将多种神经营养因子和免疫调节细胞因子直接递送至损伤部位,从而引起相应的生物学效应,并最终减缓或稳定疾病的进展。该疗法曾被FDA和EMA的授予治疗ALS的孤儿药物资格认定。
在一项评估ALS患者重复使用NurOwn的安全性和有效性的3期临床试验中显示,NurOwn在治疗ALS患者的主要和次要终点上都没有达到统计学显著性:研究结束后33%的MSC-NTF组患者和28%的安慰剂组患者达到临床反应标准(优势比=1.33,P=0.45),两组没有差异;因此,未达到主要终点。
有趣的是,尽管主要终点并没有统计学上的意义,但却在接受NurOwn治疗的患者中观察到神经炎症、神经变性和神经保护相关的脑脊液生物标记物的显著改善,以及该治疗耐受性良好等积极的因素。
除NurOwn之外,还有另一个用于治疗ALS的MSC细胞疗法lenzumestrocel (Neuronata-R)目前也正在进行三期临床试验评估。值得一提的是,Neuronata-R疗法于2014年已被韩国食品药品安全部批准用于治疗ALS。
ASO药物
◆ Ionis/Biogen : Tofersen
Tofersen是Ionis与Biogen共同研发的一种用于治疗SOD1-ALS的反义寡核苷酸药物。Tofersen可与编码SOD1的mRNA结合,使其被核糖核酸酶RNase-H降解,从而减少突变SOD1蛋白的产生。
根据在2021年10月所公布的关键III期VALOR研究结果显示,试验并未达成其主要终点,即患者根据ALS功能评分量表修订版(ALSFRS-R),自基线至试验28周评分的变化差异。但在生物活性和临床功能的多项次要和探索性终点分析显示疾病进展有减缓的趋势。根据在今年6月最新公布的12个月的整合性数据显示,早期使用tofersen可帮助持续减少神经微丝(ALS生物标志)量,并减缓多个疗效终点的下降。
在今年7月26日,FDA已接受Tofersen的新药上市申请,同时授予其优先审评资格。同时,在12月5日,EMA也接受了tofersen治疗SOD1-ALS的上市授权申请(MAA)。
◆ WAVELife Sciences:WVE-004
WVE-004是WAVELife Sciences开发的一款针对C9orf72基因突变导致的ALS和额颞叶痴呆(FTD)的ASO药物,旨在选择性靶向含有与C9orf72基因相关的六核苷酸重复扩增(G4C2)的转录变体,从而保留C9orf72蛋白。C9orf72中的G4C2扩增是ALS和FTD散发性和遗传性形式的最常见遗传原因之一。
临床前研究证明WVE-004能够强力而持久地敲减脊髓和大脑皮层中包含重复的转录物。根据对患者细胞的运动神经元和携带人类C9ORF72基因的转基因小鼠中进行测试以及进重复扩增结果显示:在小鼠的脑脊液中,6个月后,脊髓中含有重复序列的mRNA减少了60-80%,皮层中减少了40-50%。此外,WVE-004还使脊髓和皮层的二肽重复蛋白(DPR)减少了约90%,没有影响正常蛋白水平。简单来说,WVE-004可能成为对ALS抗遗传因素的一种药物。
目前,该公司正在开展WVE-004一项针对42名与C9ORF72相关的ALS或FTD患者的1/2期安全性研究。这项研究正在加拿大和荷兰的两个地点进行,预计于2023年2月完成。
AAV基因疗法
◆ Eikonoklastes Therapeutics:ET-101
ET-101(SynCav1)是Eikonoklastes授权,由加州大学圣地亚哥分校Brian Head博士实验室首创,用于过表达Caveolin-1的一种AAV9基因疗法,Caveolin-1可以组织和调节神经肌肉信号传导和功能所必需的突触受体。研究结果显示,增加Caveolin-1可以对神经细胞产生保护作用,使神经细胞可以补偿潜在疾病引起的神经退行性过程,并且使得细胞保持健康并提高其功能性。ET-101可以起到维持神经细胞健康的作用,使其成为多种神经退行性疾病的一种选择。
2022年12月,ET-101获得FDA孤儿药认定,用于治疗散发性和家族性肌萎缩侧索硬化症。目前,该疗法还尚处于临床前研究阶段。
◆ Apic Bio:APB-102
Apic Bio公司的APB-102同样是一种基因疗法候选药物,由下一代重组腺相关病毒(AAV)衣壳(rAAVrh10)和微核糖核酸(miRNA)载体组成,旨在减缓或逆转SOD1 ALS的进展。microRNA与SOD1 mRNA结合,从而减少了这种疾病患者中突变蛋白的产生。降低突变SOD1蛋白水平可能会提高运动神经元的存活率和功能,并可能为SOD1相关ALS患者提供治疗益处。临床前概念性研究已经证明APB-102可抑制突变SOD1基因活性。
此前,APB-102被FDA授予治疗SOD1 ALS的孤儿药资格认定和快速通道资格认定。目前,APB-102已经进入到IND阶段,在今年12月Eikonoklastes 还与基因疗法制造商Forge Biologics建立AAV制造合作伙伴关系,以推动ET-101进入临床试验阶段。
Treg细胞疗法
◆ Coya Therapeutics:ALS001
Coya Therapeutics公司在研的ALS001是一种自体的Treg细胞疗法,主要用于治疗ALS。其I期临床结果表明,ALS001能够对神经起到保护作用,减缓ALS的进展。2021年,ALS001曾获得FDA授予的孤儿药称号。目前,其IIa期临床试验已完成,计划将进行IIb期试验。
抗体药物
◆ Implicit Bioscience:Atibuclimab
Atibuclimab是一款靶向CD14的单克隆抗体,由小鼠可变区和人类 IgG4 Fc 区组成,可调节感染和损伤引发的致病性炎症反应。目前Atibuclimab处于2期临床研究中,旨在评估治疗ALS的安全性和有效性。2021年1月,FDA授予了Atibuclimab治疗ALS的孤儿药资格。
结语
长期以来,神经退行性疾病的治疗和缓解药物都非常有限,且效果难以让人满意,而该领域的新药研发同样是令制药行业屡屡受挫。而如今,从以上针对ALS疾病的ASO药物、AAV基因疗法和各类型细胞疗法的成功开发以及在临床试验研究中取得的良好数据,尤其是今年还迎来了第3款获批治疗ALS的药物Relyvrio,都预示着在治疗ALS上又向前跨进了一大步。
ALS或许只是一个开始,随着药企和监管机构的更多介入,可以期待未来将会有更多的神经退行性疾病受到大众关注,这类患者也能获得更多更有效更安全的治疗。
参考资料:
1.https://mp.weixin.qq.com/s?__biz=MjM5NjY5MTI4NA==&mid=2650907603&idx=1&sn=d78f8ec07475755cf2d39bf276c3c8b0&chksm=bd106fe88a67e6fe518324533257323b599556424a15594a12a03f077a640fac1660d0fc41b6&mpshare=1&scene=1&srcid=0103dCI1JcfC8y123D4tNFX0&sharer_sharetime=1672709170226&sharer_shareid=7b6ccb0dc4e247ce1c8dd4e8d8238ae6&version=4.0.20.6020&platform=win#rd
2.https://www.nature.com/articles/s41573-022-00612-2/tables/2