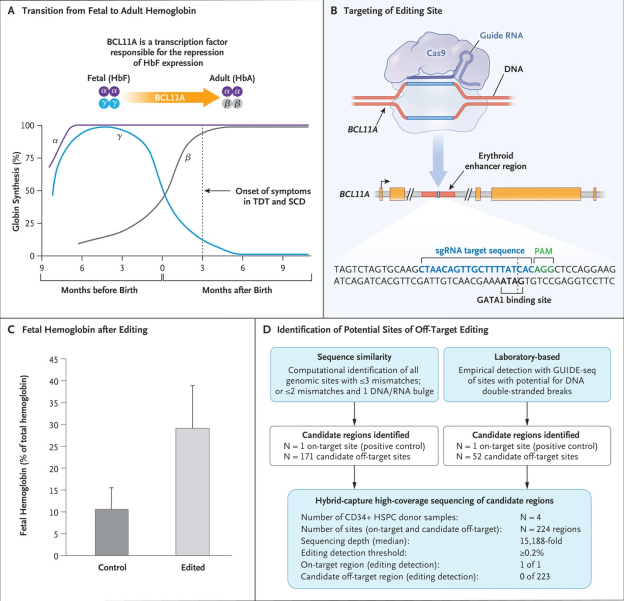
近日,欧洲药品管理局(EMA)已经受理了Vertex和CRISPR Therapeutics的CRISPR基因编辑疗法exa-cel的上市申请。exa-cel,原名CTX001™,是一种研究性、自体、体外CRISPR/Cas9基因编辑疗法,通过编辑患者自身的造血干细胞,使得患者血红细胞可以产生高水平的胎儿血红蛋白(HbF),以治疗输血依赖性β-地中海贫血(TDT)和镰状细胞病(SCD)。 HbF是携带氧气的血红蛋白的一种形式,在胚胎发育时期自然存在。婴儿出生后不久,在转录因子BCL11A的作用下,HbF便逐渐被成人血红蛋白(HbA)所替代(见图A)。因此下调BCL11A表达,可增加胎儿血红蛋白含量。 exa-cel通过应用CPRSPR-Cas9技术编辑患者自体CD34+细胞,靶向BCL11A红细胞系特异性增强子,特异性沉默BCL11A基因,重新激活HbF的产生(见图B)。exca-cel一次性输注后,HbF显著提高(见图C),且无脱靶的迹象(见图D)。试验结果表明,exa-cel不仅有可能让TDT患者摆脱长期输血的困扰,还可能缓解SCD患者镰状细胞危机和疼痛。 exa-cel的工作原理(DOI: 10.1056/NEJMoa2031054) 值得注意的是, exa-cel曾获EMA授予PRIME认证,有优先审查的资格,因此exa-cel的审查可能只需要150天,而不是210天。这意味着exa-cel有望今年在欧洲获得批准,而成为首个上市的CRISPR-Cas9治疗药物。同时Vertex和CRISPR Therapeutics业已在向美国FDA提交生物制剂许可申请(BLA),预计将在今年第一季度末完成滚动递交。 Ref: 1.https://www.biopharma-reporter.com/Article/2023/01/26/Vertex-and-CRISPR-Therapeutics-advance-towards-EMA-approval-for-exa-cel 2.https://news.vrtx.com/news-releases/news-release-details/vertex-and-crispr-therapeutics-announce-global-exa-cel 3.DOI: 10.1056/NEJMoa2031054