据国家药品监督管理局药品审评中心(CDE)官网公示,上海精缮生物科技有限责任公司(以下简称“精缮生物科技”)GC101临床试验申请获得国家药监局默示许可(受理号:CXSL2200388)。适应症为:用于隐性营养不良型大疱性表皮松解症(Recessive Dystrophic Epidermolysis Bullosa, RDEB),患者难以愈合的体表伤口的移植治疗。

而据公开资料披露,GC101是一款COL7A1转基因组织工程产品。
此前,精缮生物科技有限公司首席科学官刘敬贤在一个学术会议上做了《基因细胞治疗在大疱性疾病治疗中的应用》的报告,介绍了公司及管线,从大庖表皮松解症(RDEB)与组织工程皮肤干细胞应用、RDEB基因治疗、细胞疗法用于治疗类天疱疮前景四个方面进行了分享。
刘敬贤首先介绍了公司的主要技术,然后讲解了大庖表皮松解症(蝴蝶病)的三个亚型、临床表现、分子病因和目前的主要治疗途径,刘博士随后分享了COL7A1转基因组织工程皮肤(GC101)移植治疗RDEB的总体设计及系列验证试验。最后介绍了新的递送工具聚合物纳米粒子及治疗策略。
首个治疗方式即将诞生
大疱性表皮松解症(EB)是一种最为常见、最为严重的遗传性皮肤病,通常会导致皮肤变得脆弱和出现水疱,也称之为“蝴蝶病”。轻微的触碰或外伤就可能造成严重皮肤损伤、感染,甚至会致残。
这类疾病是由于编码表皮和基底膜带结构蛋白成分的基因突变导致,这些蛋白或合成障碍,或结构异常,从而诱发不同皮肤层解剖部位产生水泡。其中营养不良性大疱性表皮松解症(DEB)是遗传性大疱性表皮松解症中较为严重的类型,这种亚型的水疱产生在致密下层,主要与编码 VII 型胶原蛋白的基因(COL7A1)突变相关, VII 型胶原蛋白对皮肤稳定性很重要,主要作用是固定皮肤真皮层和表皮层。
当前,此类疾病还没有获批的治疗方式。常用的治疗手段包括常规治疗方式,皮肤移植和干细胞疗法等试验性疗法等,其中基因和细胞治疗是一种极具前景的方式。
而在今年8月,Krystal Biotech宣布美国食品和药物管理局(FDA)已受理该公司基因疗法产品B-VEC(beremagene geperpavec)的生物制剂许可证申请(BLA),用于治疗营养不良性大疱性表皮松解症(DEB)。该申请已经获得了优先审评资格,其PDUFA日期定于2023年2月17日。

B-VEC是一种研究性的非侵入性、局部给药并且可重复给药的基因疗法,使用经基因工程改造而来的复制缺陷型HSV-1载体,包含两个COL7A1基因的拷贝片段,为患者的皮肤细胞提供模板来制造正常的VII型胶原蛋白(COL7)蛋白,通过恢复DEB患者角质形成细胞和成纤维细胞中COL7的表达来实现治疗作用。该药物采用凝胶剂型设计,可以由皮肤科医生或初级护理医师直接应用于患者皮肤DEB伤口处,促进伤口愈合。
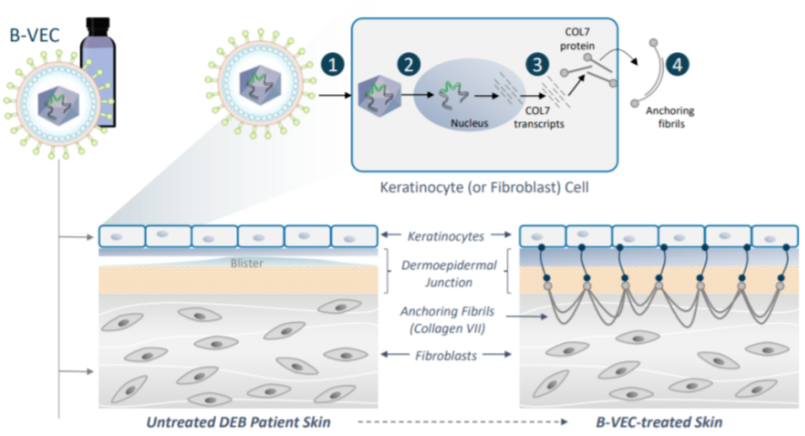
B-VEC作用机制 图源:Krystal官网
该BLA得到两项含安慰剂对照的临床试验GEM-3和GEM-1/2的支持。关键性GEM-3临床试验共招募了31例DEB患者,在治疗3个月时与安慰剂相比71%接受B-VEC治疗的患者伤口完全愈合,在治疗6个月时67%接受B-VEC治疗的患者伤口完全愈合,该临床试验达到了其主要终点。如果获得批准,B-VEC将成为治疗DEB的首款获批疗法。
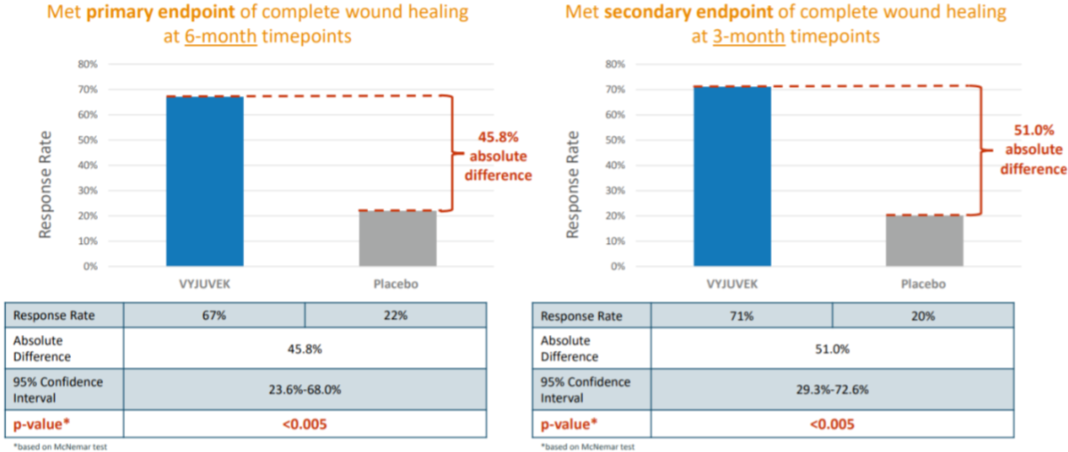
GEM-3临床试验数据 图源:Krystal官网
同年11月,Abeona Therapeutics宣布了其关键3期VIITAL™研究的积极顶线数据,该研究评估了EB-101治疗隐性营养不良性大疱性表皮松解症(RDEB)患者的安全性和有效性,并达到了两个共同主要疗效终点。

EB-101是一种自体、基因纠正的细胞疗法,将COL7A1基因导入患者自身皮肤细胞(角质形成细胞)并将其移植回患者体表,以纠正COL7A1基因,正常表达VII型胶原蛋白,从而促进伤口愈合。该疗法已获得欧盟和FDA授予的孤儿药资格。
VIITAL™研究中随机分配治疗11名患者大于20平方厘米的慢性伤口,保持开放至少六个月,最长21年(平均6.2年)。在六个月时间点时,EB-101治疗与对照组相比有着显著的伤口愈合改善,随机治疗伤口愈合比率达81.4%。同时,这一疗法还减轻了患者的疼痛,平均疼痛较基线减轻3.07。在安全性方面,无严重治疗相关不良事件发生,药物耐受性良好。
基于此,Abeona计划在2023年第二季度向美国FDA提交生物制品许可申请(BLA)。若顺利获批,EB-101有望成为首款获FDA批准的治疗RDEB自体工程细胞疗法。
参考资料:
1.CDE官网