AAV基因治疗药物“GC101腺相关病毒注射液”获得了国家药监局药审中心的临床试验默示许可,注册分类为1类,受理号为:CXSL2200400,适应症为2型脊髓性肌萎缩症(2型SMA),这是继10月8日该药的适应症-1型SMA获批后的又一新适应症获批。
据悉,药监局药审中心分别于7月19日及8月25日受理了GC101注射液用于1型SMA和2型SMA的临床试验注册申请。
除了GC101,锦篮基因的GC304腺相关病毒注射液也于同日获得临床试验默示许可,可谓双喜临门!此外,锦篮基因针对婴儿型庞贝病的基因治疗药物GC301的研究者发起的临床研究也已于9月份顺利完成首例患者给药,期待早日听到更多好消息!
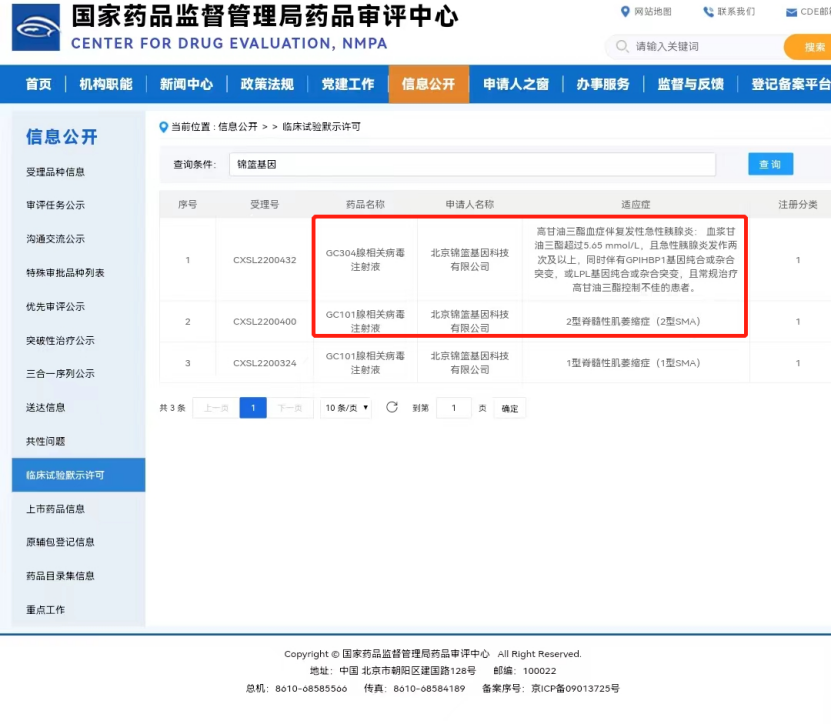
| 关于脊髓性肌萎缩症
脊髓性肌萎缩症(spinal muscular atrophy,SMA)是一组脊髓前角细胞变性、导致对称肌无力和肌萎缩为特征的常染色体隐性遗传的神经肌肉疾病,为一种常见的运动神经元疾病,SMA患者的典型变现是肌无力、肌张力低、肌萎缩,正常站立、行走等运动功能受限等,运动发育显著落后于正常儿童,甚至无法完成如咀嚼、吞咽、呼吸等一些维持生命活动的最基本动作,但智力发育正常。任何年龄、种族、性别的人都有可能患上SMA,SMA新生儿发病率在1/5000–1/10000,SMA产前携带率为1/35-1/50,家庭高危率约1/1600。
| 关于GC101注射液
GC101注射液可通过鞘内给药方式直接向中枢神经系统递送和补充SMN蛋白,从而改善SMA患者呼吸功能及运动能力。