杜氏肌营养不良症,1861年由法国医生Duchenne发现,是目前人类已知遗传病中由于最大、最复杂的基因缺陷所导致的致死性疾病,随着年龄增加全身肌肉进行性退化、运动功能减退,为X-连锁遗传病。被列入罕见病范围,其发病率约1/3800~1/6000活产男婴,是肌营养不良中发病率最高、病情最为严重的一型。

一、临床表现
在婴儿期和儿童早期通常无症状或表现为轻微的运动发育延迟,血清肌酸激酶(CK)增高。此期诊断较困难,可在体检中偶然发现或由于阳性的家族史而发现。患者一般在4周岁左右出现肌无力症状,此后进行性加重。
患者肌肉损伤首先发生在下肢,逐渐累及其它肌群,从仰卧位起立困难,出现典型Gowers征表现。受损害的肌肉萎缩,但脂肪含量增加,出现假性肥大,腓肠肌受累最为明显。腓肠肌假性肥大是该病相对特征性表现之一。脊柱侧凸也很常见,其它表现为步态异常、易摔跤、上楼困难、起蹲困难、轻中度智力落后等症状。
大多数患儿13岁后无法独立步行,需要依靠轮椅。随着年龄的增长,一些患者出现心肌病,呼吸功能下降,20~30岁死于心、肺功能衰竭,很少能存活到30岁以上。
根据杜氏肌营养不良症患者症状出现的时序性特点,Bushby等将杜氏肌营养不良症临床经过分为5个阶段:
第一阶段(症状前期):偶然发现血清肌酶升高或有家族史,可能在本阶段会被诊断,此阶段患儿可能运动智力发育迟缓,爬、独走的时间较同龄儿延迟,没有步态异常。
第二阶段(早期独走期):一般在5岁前发病,多数从3~4岁开始出现肢体无力,上台阶费力,蹲起费力,跑步缓慢,行走姿势异常,摇摆呈鸭步,走路时足尖着地,Gowers征阳性,腓肠肌肥大,双膝腱反射减弱或消失。
第三阶段(晚期独走期):一般7岁后病情进展加速,走路日渐困难,丧失爬楼梯和仰卧起立的能力,不能完成Gowers征,跟腱挛缩加重,部分患者膝关节挛缩,少数患者出现髋关节的半脱位或脱位。
第四阶段(早期不能独走期):下肢肌力继续下降,通常在10岁左右丧失独立行走能力,可以短距离扶行、独坐或扶站,髋关节半脱位或脱位,膝关节挛缩加重,肘关节开始挛缩,出现脊柱侧弯,腓肠肌逐渐萎缩。
第五阶段(晚期不能独走期):通常14~15岁后不能独坐,双上肢活动开始受限。发病越早,呼吸与心脏功能损害越明显,由于呼吸肌无力发生无效咳嗽、夜间低通气、睡眠呼吸紊乱,最终导致呼吸衰竭。多数患者因呼吸或心力衰竭在30岁前死亡。
二、病因
DMD基因是目前已知人类最大的基因,主要作用是产生抗肌营养不良蛋白(dystrophin),该蛋白主要在骨骼肌和心肌细胞膜内面表达,是一种细胞骨架蛋白,其主要作用是稳定和保护肌纤维。
DMD基因致病性变异最终会导致抗肌营养不良蛋白的缺乏或减少,肌纤维的完整性遭到破坏,进而引发肌纤维坏死、肌肉纤维化和再生能力丧失,严重者可见纤维结缔组织和脂肪组织替代正常的肌肉组织,出现肌肉假性肥大的典型表现。
为什么说传男不传女?
正常情况下,人类有23对染色体,其中1-22对为常染色体,是男性和女性共有的;最后一对随男、女性别而异,称性染色体,女性为XX,男性为XY。
DMD是一种X连锁隐性遗传病,致病DMD位于X染色体上,由于男性只有一条X染色体,因此该基因若出现致病变异则可发病;女性因为有两条X染色体,一般只是致病变异的携带者.
若女性发病,需考虑以下几种可能的情况:
1、DMD基因发生纯合或复合杂合突变;
2、X染色体发生差异性失活,即未发生DMD基因突变的X染色体失活,而携带DMD基因突变的X染色体未失活;
3、单亲二体或X单体;
4、X染色体复杂重排;
5、社会性别为女性,染色体核型为46,XY的两性畸形患者等。
以上情况很少见,因此男性比女性更容易患DMD,即所谓的“传男不传女”。
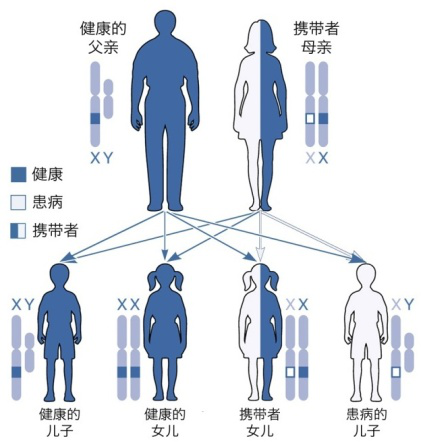
图1:X连锁隐性遗传方式
男性患者的DMD基因致病变异多来自携带该遗传变异的母亲。
备孕夫妻可表型正常,但女性DMD基因致病突变携带者的后代中:男性有50%可能患病,50%可能正常;女性50%可能为携带者,50%可能不携带致病突变。
男性DMD患者通常由于过早死亡或病情较重无法生育后代,若患者能够生育,并且他的妻子不携带DMD基因致病变异,那么他们的后代中男性不会患病,女性必定是携带者。
三、诊断
在出现症状后可以根据临床表现及血清肌酶、肌电图、肌肉病理对杜氏肌营养不良症进行诊断。基因检测是确诊杜氏肌营养不良症的主要方法。
DMD基因定位于Xp21,长2500kb,包括79个外显子、78个内含子和8个启动子。DMD基因缺陷导致骨骼肌中其编码蛋白dystrophin的缺失,基因突变形式多样,其中大片段缺失约占杜氏肌营养不良症患者65%;大片段重复约占5%~10%;
其余突变为微小突变,包括碱基的缺失、插入、置换、内含子突变、复杂的染色体重排等。远端外显子45~55和近端外显子2~20是两个缺失、重复的热点部位。

四、治疗
1. 药物治疗
糖皮质激素是治疗杜氏肌营养不良症的传统药物,强的松或其他糖皮质激素治疗可以帮助患者延长行走时间,降低脊柱侧弯的发生率,延迟呼吸衰竭的发生,可延长10~20年的寿命。
2. 基因治疗
越来越多针对杜氏肌营养不良症的基因治疗研究获得了有效证据,如基因替代疗法、基因产物修饰、相关蛋白调控等,正在或已经进入了临床前试验阶段或临床试验,部分患者治疗后肌肉组织恢复了正常dystrophin蛋白表达,不仅病程减缓,患者的生存时间延长,生活质量有所提高。此类临床试验的成功将为杜氏肌营养不良症的有效治疗带来希望。
3. 骨髓干细胞移植
自体骨髓干细胞移植疗法可在近期增加患者肌力、提高生活能力、改善运动功能。
4. 营养及对症支持治疗
高蛋白高维生素、低碳水化合物饮食有助于改善肌肉质量,预防肥胖。维生素D、钙磷、左卡尼汀等支持治疗有助于保护骨骼及心肌功能,减缓骨关节病变等合并症。
五、预防护理
预防进行性肌营养不良的有效手段是遗传咨询、产前诊断和选择性流产。在先证者明确的基因诊断基础上,可对家族成员进行携带者筛查,母亲再次妊娠时进行胎儿基因诊断,以减少家族中相同疾病患儿的出生。
日常生活中应注意防护,避免外伤、疲劳及交叉感染。鼓励户外活动,晒太阳。鼓励游泳、温水浴,改善肌肉及骨关节功能。

参考文献:
北京医学会罕见病分会,北京医学会神经内科分会神经肌肉病学组,中国肌营养不良协作组. Duchenne型肌营养不良多学科管理的专家共识.中华医学杂志.2018,98(35):2803-2814.
Verhaart Ingrid E C,Aartsma-Rus Annemieke. Therapeutic developments for Duchenne muscular dystrophy [J]. Nature reviews. Neurology,2019.
陈远春,宋燕,谭书江.杜氏肌营养不良基因治疗策略研究进展[J].儿科药学杂志,2019,25(02):64-66.
杨茹莱.杜氏肌营养不良临床特点及诊治进展[J].中国儿童保健杂志,2018,26(03):233-235.