
近日,一家专注于基因疾病和癌症的商业阶段生物制药公司BridgeBio宣布,其基于腺相关病毒AAV9的基因疗法BBP-812已在第1/2期临床试验中完成首例患者给药,用于治疗卡纳文病(Canavan)。
Canavan是一种极其罕见和致命的疾病,由天冬氨酸酰化酶(ASPA)基因突变引起致死性脑白质营养不良,没有 ASPA 产生的酶,大脑将无法正确形成在脑内传递信号的神经束。结果就是患儿不会说话或无法控制自己的四肢,并且他们的认知能力也受到了限制。这种疾病在美国约影响到大约1,000名儿童,目前既没有治愈的方法,也没有批准的治疗方法。

Canavan病患者(图片来源:麻省理工科技评论)
BBP-812是一种针对Canavan的AAV9基因治疗方法。重组腺相关病毒(RAAV)具有跨越血脑屏障和广泛转导中枢神经系统的能力,BridgeBio应用AAV基因治疗,寻将提供功能副本的ASPA基因贯穿全身,并进入大脑,这种方式有可能从源头上纠正疾病。
Canavan病模型的临床前概念证明结果表明,恢复存活和正常运动功能的途径是可行的。随后,BBP-812获得了美国食品和药物管理局授予快车道指定、罕见儿科药物指定和孤儿药物指定,同时也被欧洲药品管理局授予孤儿药物的称号。
正在进行的第1/2期开放标签研究旨在评估BridgeBio的AAV 9基因疗法BBP-812的安全性、耐受性和药效学活性。在研究的初始剂量发现阶段,每个病人将接受一次静脉滴注BBP-812。这项研究的主要结果是安全性,以及尿和中枢神经系统N-乙酰天冬氨酸(NAA)水平的变化,运动功能和发展也将得到评估。1/2期临床实验的初步数据预计在2022年发布。
“根据我们在临床前研究中观察到的疗效和安全性数据,我们希望我们的研究基因疗法能够成为治疗卡纳万儿童的一个有意义的选择。目前,这些儿童只能获得支持性的治疗,因为目前还没有批准的治疗方法来治疗这种破坏性疾病。”亚当·夏维茨博士,BridgeBio基因治疗公司首席医官。
在我们的Canavan疾病试验中给第一位病人服用药物是我们基因治疗团队的一项重大成就,如果没有我们在病人、医学和科学界的合作伙伴的支持,我们就不会在这里。”埃里克·大卫供职于BridgeBio基因治疗公司的首席执行官J.D.。“我们致力于加拿大社区,并将致力于推进这一试验和我们基因治疗组合中的其他项目,因为我们深信基因疗法在改善和挽救生命方面的潜力。”
BridgeBio对Canavan病的AAV 9基因治疗研究是该公司为患有遗传病和基因驱动的癌症的患者提供临床或商业环境的14个项目之一。
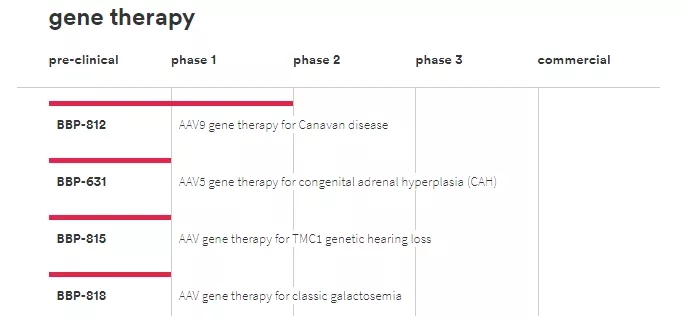
BridgeBio基因治疗在研管线(图片来源:BridgeBio官网)
AAV的来源与发展
腺病毒相关病毒(AAV)最早是在20世纪60年代中期从实验室腺病毒(AdV)制剂中发现的,并且很快就在人体组织中发现。
在纯科学的好奇心驱使下,一些研究小组开始了解基本AAV生物学的过程,此时并没有意识到其作为人类基因治疗平台的巨大潜力。在AAV研究的前15-20年中,AAV的几个重要方面被表征,包括其基因组构型和组成、DNA复制和转录、感染潜伏期和病毒粒子组装。这些成果共同促进了野生型AAV2序列成功克隆到质粒中,从而实现了基因研究和整个AAV2基因组测序。早期研究提供了使用AAV作为基因传递载体的基础知识。
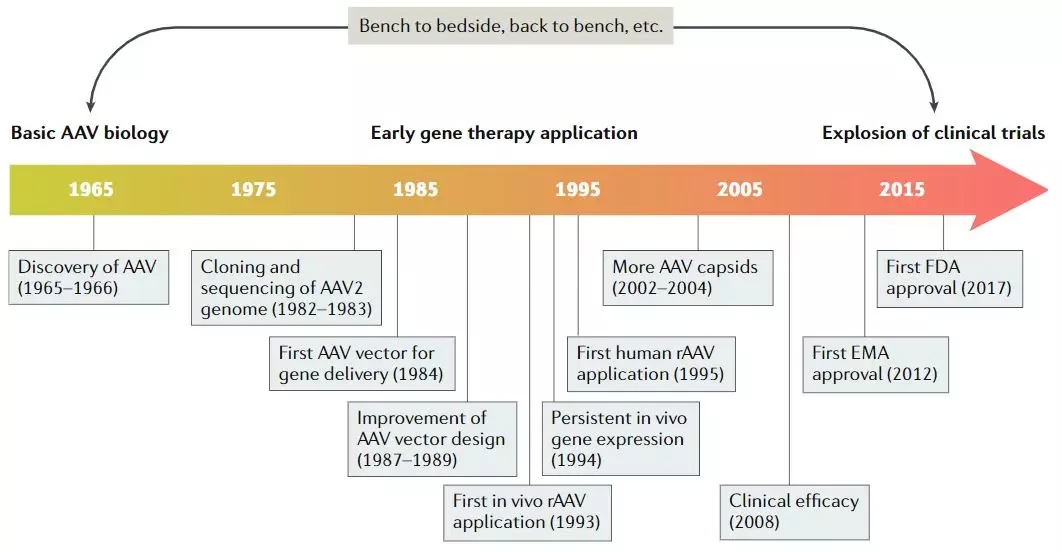
50年AAV时间线(图片来源:Nature Reviews Drug Discovery )
现如今,重组AAV(rAAV)已经成为体内基因治疗递送的主要平台。考虑到AAV的天然趋向性和未满足的医疗需求,大多数rAAV基因治疗计划集中于肝脏、横纹肌和中枢神经系统(CNS)。
几乎所有天然AAV衣壳都可以在全身给药后有效地转导肝脏。因此,rAAVs提供了一个强大的肝靶向平台来治疗各种疾病,如A型血友病和B型血友病、家族性高胆固醇血症、鸟氨酸转氨甲酰酶缺乏症和Crigler-Najjar综合征。
诸如AAV8和AAV9的衣壳,可以靶向全身的多种肌肉类型,使得能够针对多种肌肉疾病开发rAAV基因疗法,特别是那些影响全身肌肉的疾病,例如DMD。值得注意的是,转导的肌肉可以作为生物工厂来产生用于治疗非肌肉疾病的分泌治疗性蛋白质。
此外,虽然大多数心脏病是多基因的并且受环境因素的影响,但已经测试了几种参与信号传导和代谢的基因来治疗心力衰竭。
临床开发中大部分的rAAV基因疗法集中在CNS,包括大脑和眼睛。
眼睛是一种封闭的和分隔的器官,这促使rAAV基因的局部递送。值得注意的是,FDA批准的第一种rAAV基因治疗药物Luxturna,用于治疗患有由RPE65基因突变引起的遗传性视力丧失的患者。
相比之下,大脑更复杂,更大。直接脑实质内rAAV注射可以促使rAAV的局部分布,并且理想地用于治疗影响脑部限定区域的CNS疾病,例如帕金森病中的壳核。另一方面,通过鞘内注射递送到脑脊液空间可以实现更广泛的CNS分布。不幸的是,这些给药途径可能是侵入性的并且带来潜在的风险。
或者,静脉内递送某些血清型载体,例如AAV9和AAVrh.10,使载体穿过血脑屏障(BBB)以转导神经元和神经胶质细胞。这一具有里程碑意义的发现促成了一系列研究,证明了全身性rAAV给药的治疗效果,其目标是影响CNS广泛区域的疾病,包括脊髓性肌萎缩症(SMA)、肌萎缩侧索硬化、Canavan病、GM1 ganglio-sidosis和粘多糖贮积症III型。利用这种强大的rAAV平台的多项基因治疗临床试验目前正在进行中。
版权声明:本网站所有注明“来源:罕见病信息网”的文字、图片和音视频资料,版权均属于罕见病信息网网站所有。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。